题目内容
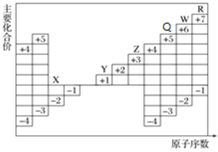
【题目】如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是其中的五种元素。下列说法不正确的是
A.离子半径:Y>X
B.33号砷元素与Q同族
C.最高价氧化物的水化物的酸性:R>W
D.单质与水(或酸)反应的剧烈程度:Y>Z
【答案】A
【解析】
短周期主族元素中,X只有-2价,没有正化合价,则X为O元素;Y为+1价,没有负化合价,原子序数大于氧,则Y为Na;Z为+3价,没有负化合价,原子序数大于Na,故Z为Al;Q化合价由+5、-3,Q是P元素;W有+6、-2价,则Z为S元素;R有+7、-1价,则R为Cl。
A.电子层数相同,质子数越多半径越小,离子半径:O2->Na+ ,故A错误;
B.33号砷元素最外层有5个电子,属于ⅤA族元素;Q是P元素,属于ⅤA族元素,故B正确;
C.非金属性Cl>S,最高价氧化物的水化物的酸性HClO4>H2SO4,故C正确;
D.金属性Na>Al,与水(或酸)反应的剧烈程度Na>Al,故D正确;
选A。

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目