题目内容
欲用质量分数为98%的浓硫酸(ρ=1.84 g/cm3)配制成浓度为0.5 mol/L的稀硫酸500 mL.
(1)选用的主要仪器有________.
(2)请将下列各操作,按正确的序号填在横线上.
A.用量筒量取一定体积的浓H2SO4
B.反复颠倒摇匀
C.加蒸馏水至距刻度2~3 cm时,改用胶头滴管加水至刻度
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液一并转移至容量瓶,摇匀
E.在烧杯中稀释浓H2SO4
F.静置,待溶液恢复至室温后,将溶液转入容量瓶
G.将所配溶液转移至洁净干燥的试剂瓶,并贴上标签
其操作正确的顺序依次为________.
(3)简要回答下列问题:
①所需浓硫酸的体积为________mL.
②如果实验室有15 mL、20 mL、50 mL的量筒应选用________mL的量筒最好,量取时发现量筒不干净用水洗净后直接量取会使浓度________.
③将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并不断搅拌的目的是________,若搅拌过程中有液体溅出会使浓度偏________.
④在转入容量瓶前烧杯中液体应________,否则会使浓度________;并洗涤烧杯2~3次,洗涤液也要转入容量瓶,否则会使浓度________.
⑤定容时必须使溶液凹液面与刻度相平,若俯视结果会使浓度________;仰视则使浓度________.
解析:
|
答案:(1)量筒、烧杯、玻璃棒、500 mL容量瓶、胶头滴管 (2)A、E、F、D、C、B、G (3)①13.6 ②15,偏低 ③迅速散热,防止暴沸,低 ④静置冷却,偏高,偏低 ⑤偏高,偏低
|
提示:
|
该题为配制一定物质的量浓度方面的综合应用题,它涉及计算、配制步骤、仪器选择、误差分析等多个方面的内容,能力要求比较高.只有平时对知识深刻理解,并善加应用,才能完全解题. |

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
 欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液480mL.试回答下列问题:
欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液480mL.试回答下列问题: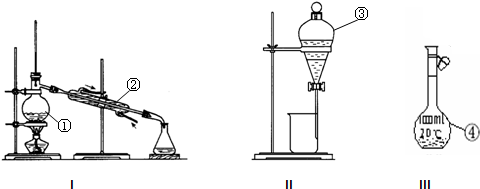
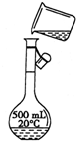 欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液500mL.试回答下列问题:
欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液500mL.试回答下列问题: