题目内容
19.下列反应中,离子方程式为H++OH-=H2O的是( )| A. | CH3COOH+NaOH═CH3COONa+H2O | B. | HNO3+KOH═KNO3+H2O | ||
| C. | 3HCl+Fe(OH)3═FeCl3+3H2O | D. | 2HCl+Cu(OH)2═CuCl2+2H2O |
分析 H++OH-=H2O表示强酸或者强酸的酸式盐与强碱反应生成水、可溶性盐,据此解答.
解答 解:A.醋酸为弱电解质,应保留化学式,CH3COOH+NaOH═CH3COONa+H2O的离子方程式:CH3COOH+OH-=CH3COO-+H2O,故A错误;
B.HNO3+KOH═KNO3+H2O,反应的离子方程式:H++OH-=H2O,故B正确;
C.氢氧化铁为沉淀,应保留化学式,离子方程式为:3H++Fe(OH)3═Fe3++3H2O,故C错误;
D.氢氧化铜为沉淀,离子方程式为:3H++Cu(OH)2═Cu2++2H2O,故D错误;
故选B.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意化学式的拆分,题目难度不大.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
10.下列反应中,既属于氧化还原反应,同时又是吸热反应的是( )
| A. | Ba(OH)2•8H2O与NH4Cl的反应 | B. | 铝与盐酸的反应 | ||
| C. | 强酸和强碱反应生成水的反应 | D. | 灼热的炭与二氧化碳的反应 |
7.向明矾[KAl(SO4)2]溶液中滴入氢氧化钡溶液,当硫酸根离子恰好完全沉淀时,铝元素的存在形式是( )
| A. | 一部分为A1(OH)3,一部分为Al3+ | B. | 一部分为Al(OH)3,一部分为A1O2- | ||
| C. | 全部是Al(OH)3 | D. | 全部是A1O2- |
14.下列说法正确的是( )
| A. | 将CO2通入溶有足量氨气的BaCl2溶液中,无白色沉淀生成 | |
| B. | 将盐酸、KSCN溶液和Fe(NO3)2溶液三种溶液混合,混合溶液显红色 | |
| C. | 石蕊试纸和pH试纸使用前都必须用蒸馏水润湿 | |
| D. | 浓硫酸有氧化性,稀硫酸没有氧化性 |
4.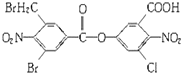 已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )
已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )
 已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )
已知某有机物结构简式如图:1mol该有机物与足量NaOH溶液共热,充分反应最多可消耗a mol NaOH,则a值是( )| A. | 6 mol | B. | 7 mol | C. | 8 mol | D. | 9 mol |
8.设NA为阿佛加德罗常数,下列叙述中正确的是( )
| A. | 46gNO2和 N2O4混合气体中含有原子总数为3NA | |
| B. | 标准状况下22.4LH2中含中子数为2NA | |
| C. | 7.1k氯气与足量NaOH溶液反应转移的电子数为0.2NA. | |
| D. | 1molC10H22分子中共价键总数为62 NA |
18.合成氨工业中氢气可由天然气和水反应制备,其主要反应为:CH4(g)+2H2O(g)?CO2(g)+4H2(g)
已知,破坏1mol化学键需要吸收的热量如下表所示:
试通过计算判断,下列有关甲烷转化成氢气过程的能量变化示意图正确的是( )
已知,破坏1mol化学键需要吸收的热量如下表所示:
| 化学键 | C-H | O-H | C=O | H-H |
| 吸收热量(kJ/mol) | 414 | 464 | 803 | 436 |
| A. | 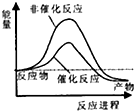 | B. | 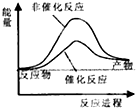 | C. | 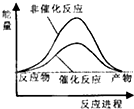 | D. | 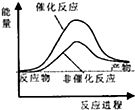 |
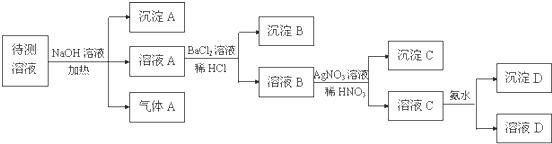
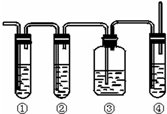 实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4生成少量的SO2,有人设计下列实验以确认上述混合气体中有乙烯和SO2,试回答下列问题:
实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4生成少量的SO2,有人设计下列实验以确认上述混合气体中有乙烯和SO2,试回答下列问题: