题目内容
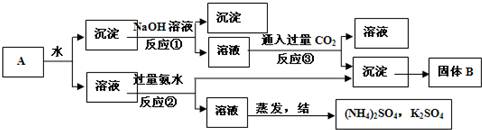
在一定条件下可实现如图所示的变化。
请完成下列各题:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解。上图中的F是_________。
(2)写出明矾溶液与过量的NaOH溶液反应的离子方程式______________________________。
(3)图中所得G和D都为固体,混合物在高温下可发生反应,写出该反应的化学方程式:_________________________________________。
(4)每生成1 mol D,同时生成_______________mol E。
(1)CO2
(2)Al3++4OH-![]()
![]() +2H2O
+2H2O
(3)3CuO+2Al![]() 3Cu+Al2O3
3Cu+Al2O3
(4)0.75
解析:解答本题要将框图中的信息和问题中的信息结合起来,孔雀石分解的产物是CuO、CO2和H2O,明矾〔KAl(SO4)2〕溶于过量的NaOH溶液所得的A中主要成分是NaAlO2,因为A与F反应可得沉淀,则F必为CO2,G为CuO,且所得的沉淀为Al(OH)3。Al(OH)3加热分解得Al2O3和H2O,则B为Al2O3。因为D为固体,则D是Al,E是O2,此步反应的条件是电解。联系到Al能与金属氧化物发生铝热反应的性质,可知Al与CuO在高温下发生的反应也是铝热反应,产物为Al2O3和Cu。根据电解Al2O3的方程式:2Al2O3![]() 4Al+3O2,由得失电子数相等的原理可知每生成1 mol D,同时生成E的物质的量为:
4Al+3O2,由得失电子数相等的原理可知每生成1 mol D,同时生成E的物质的量为:![]() =0.75 mol。
=0.75 mol。

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目