题目内容
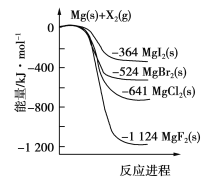
【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是
A.由MgCl2制取Mg是放热过程
B.热稳定性:MgI2>MgBr2>MgCl2>MgF2
C.常温下氧化性:F2<Cl2<Br2<I2
D.由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2(s)+Cl2(g)===MgCl2(s)+Br2(g),ΔH=-117 kJ·mol-1
【答案】D
【解析】A项分析图像可知,MgCl2的能量低于Mg与Cl2的能量之和,依据能量守恒定律知由MgCl2制取Mg的反应为吸热反应;B项,物质的能量越低越稳定,化合物的稳定性顺序为:MgI2<MgBr2<MgCl2<MgF2;C项,同主族元素从上到下,非金属性减弱,则单质的氧化性的顺序为:F2>Cl2>Br2>I2;D项,分析图像可知反应的焓变等于-117 kJ·mol-1。

练习册系列答案
相关题目