题目内容
11.下列说法正确的是( )| A. | 浓度为0.1mol•L-1 CH3COOH溶液,加水稀释,则$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 浓度为0.1mol•L-1 CH3COOH溶液,升高温度,Ka (CH3COOH)不变,但醋酸的电离程度增大 | |
| C. | 在稀AgNO3溶液中先加入过量0.1mol/L NaCl溶液,再加入少量0.1mol/L Na2S溶液,先产生白色沉淀,后出现黑色沉淀,说明Ksp(AgCl)>Ksp(Ag2S) | |
| D. | 在恒容密闭容器中,反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0达到平衡后,使用高效催化剂,正反应速率增加,逆反应速率减小,平衡正向移动 |
分析 A、醋酸溶液加水稀释,平衡正向移动,n(CH3COO-)增大,n(CH3COOH)减小;
B、温度升高,醋酸的电离平衡正向移动,电离平衡常数增大;
C、AgCl、AgI均不溶于水,但AgI的溶解度更小;
D、催化剂能够同等程度的增大正逆反应速率,不影响平衡移动.
解答 解:A、醋酸溶液加水稀释,醋酸根离子和醋酸分子浓度都减小,平衡正向移动,n(CH3COO-)增大,n(CH3COOH)减小,所以$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$增大,故A错误;
B、温度升高,醋酸的电离程度增大,Ka (CH3COOH)增大,故B错误;
C、在稀AgNO3溶液中先加入少量0.1mol/L NaCl溶液,再加入少量0.1mol/L NaI溶液,发生沉淀的转化,先产生白色沉淀,后出现黄色沉淀,则说明Ksp(AgCl)>Ksp(AgI),故C正确;
D、催化剂能够同等程度的增大正逆反应速率,使用高效催化剂,正反应速率增加,逆反应速率增大,平衡不移动,故D错误;
故选C.
点评 本题考查了弱电解质加水稀释时离子浓度变化、温度对醋酸电离平衡的影响、沉淀的转化以及催化剂对反应速率和平衡的影响,题目难度不大.

练习册系列答案
相关题目
1.下列反应能说明卤素非金属性活泼顺序是Cl>Br>I的是( )
①2HClO4+Br2(气)═2HBrO4+Cl2?②2ΝαΒr+Cl2═2NaCl+Br2 ③2KI+Cl2═2KCl+I2 ④2KI+Br2═2KBr+I2.
①2HClO4+Br2(气)═2HBrO4+Cl2?②2ΝαΒr+Cl2═2NaCl+Br2 ③2KI+Cl2═2KCl+I2 ④2KI+Br2═2KBr+I2.
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①②③④ |
2.下列工业生产过程中涉及不到氧化还原反应的是( )
| A. | 接触法制硫酸 | B. | 侯德榜制纯碱 | ||
| C. | 粗铜精炼 | D. | 石油的裂化和裂解 |
6.向13.6由Cu和Cu2O组成的混合物中加入一定浓度的稀硝酸250mL,当固体物质完全溶解后生成Cu(NO3)2和NO气体.在所得溶液中加入0.5mol.L-1的NaOH溶液1.0L,生成沉淀质量为19.6g,此时溶液呈中性且金属离子已完全沉淀.下列有关说法正确的是( )
| A. | 原固体混合物中Cu与Cu2O的物质的量之比为1:1 | |
| B. | 原稀硝酸中HNO3的物质的量浓度为1.3mol•L-l | |
| C. | 产生的NO的体积为2.24L | |
| D. | Cu、Cu2O与硝酸反应后剩余HNO3为0.1mol |
3.某单质甲及其化合物乙、丙、丁、戊在一定条件下发生如图所示的变化,乙可以是( )


| A. | PH3 | B. | H2S | C. | HCl | D. | NH3 |
1.元素周期表的一部分,表中的①--⑩中元素,回答下列填空:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)非金属性最强的元素是氟(填元素名称)
(3)写出①⑦对应两种元素的符号分别为N、Cl,(填元素符号)元素③⑤的最高价氧化物对应的水化物相互反应的离子方程式为Al(OH)3+OH-=AlO2-+H2O
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是(填对应化合物的化学式,下同)HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)写出确定某一溶液中含有元素⑨存在的实验操作:用洁净的铂丝蘸取少量待测试样于酒精灯外焰灼烧,透过蓝色钴玻璃观察火焰的颜色,火焰呈紫色,说明该试样含有K+.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)非金属性最强的元素是氟(填元素名称)
(3)写出①⑦对应两种元素的符号分别为N、Cl,(填元素符号)元素③⑤的最高价氧化物对应的水化物相互反应的离子方程式为Al(OH)3+OH-=AlO2-+H2O
(4)这些元素中的最高价氧化物对应的水化物中,酸性最强的是(填对应化合物的化学式,下同)HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(5)写出确定某一溶液中含有元素⑨存在的实验操作:用洁净的铂丝蘸取少量待测试样于酒精灯外焰灼烧,透过蓝色钴玻璃观察火焰的颜色,火焰呈紫色,说明该试样含有K+.

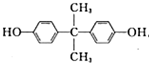 ,G是一种高分子,可用于制造隐形眼镜的材料.H为六元环酯.
,G是一种高分子,可用于制造隐形眼镜的材料.H为六元环酯. .
. .
. .
.