题目内容
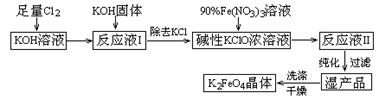
(12分)纳米ZnS具有独特的光电效应,在电学、磁学、光学等领域应用广泛。以工业废渣锌灰(主要成分为Zn、ZnO,还含有Fe2O3、FeO、CuO等杂质)为原料制备纳米ZnS的工业流程如下:

请回答下列问题。
(1)酸浸时FeO与稀HNO3反应的离子方程式 。
(2)将酸浸的尾气循环利用,加入的X气体可以是 。
(3)流程中加入ZnO调pH的目的是 。
(4)滤渣2中的成分是 。
(5)已知ZnS的溶度积Ksp=1.6×10-24,溶液中Zn2+浓度为0.01mol·L-1,则溶液中S2—浓度大于 mol·L一1,才生成ZnS沉淀。
(6)试设计简单实验方案,判断所得ZnS样品颗粒是否为纳米级 。

请回答下列问题。
(1)酸浸时FeO与稀HNO3反应的离子方程式 。
(2)将酸浸的尾气循环利用,加入的X气体可以是 。
(3)流程中加入ZnO调pH的目的是 。
(4)滤渣2中的成分是 。
(5)已知ZnS的溶度积Ksp=1.6×10-24,溶液中Zn2+浓度为0.01mol·L-1,则溶液中S2—浓度大于 mol·L一1,才生成ZnS沉淀。
(6)试设计简单实验方案,判断所得ZnS样品颗粒是否为纳米级 。
(1)3FeO+10H++NO3—=3Fe3++NO+5H2O (2分)
(2)空气(或O2) (2分)
(3)除去溶液中的Fe3+ (2分)
(4)Cu、Zn (2分)
(5)1.6×10—22 (2分)
(6)取少量样品和水混合形成分散系,让一束光照射,若出现一条光亮的通路,则是纳米级,否则不是。 (2分)
(2)空气(或O2) (2分)
(3)除去溶液中的Fe3+ (2分)
(4)Cu、Zn (2分)
(5)1.6×10—22 (2分)
(6)取少量样品和水混合形成分散系,让一束光照射,若出现一条光亮的通路,则是纳米级,否则不是。 (2分)
试题分析:(1)HNO3把FeO氧化为Fe3+,HNO3被还原为NO,配平可得离子方程式:3FeO+10H++NO3—=3Fe3++NO+5H2O
(2)NO与O2、H2O反应可生成HNO3,实现尾气循环利用,所以X气体为空气(或O2)。
(3)加入硝酸后,与Fe2O3、FeO反应生成Fe3+,流程中加入ZnO调pH可使Fe3+转化为Fe(OH)3沉淀,所以加入ZnO调pH的目的是除去溶液中的Fe3+
(4)加入Zn后,Zn与Cu2+反应生成Cu,所以滤渣2中的成分是Cu、Zn
(5)c(S2?)= Ksp÷c(Zn2+)=1.6×10-24÷0.01=1.6×10—22mol?L?1,所以溶液中S2—浓度大于1.6×10—22mol?L?1,才生成ZnS沉淀。
(6)纳米级颗粒与水混合可形成胶体,具有丁达尔效应,所以实验方案为:取少量样品和水混合形成分散系,让一束光照射,若出现一条光亮的通路,则是纳米级,否则不是。sp的计算。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目