题目内容
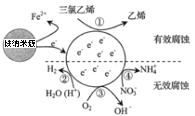
【题目】目前认为酸催化乙烯水合制乙醇的反应机理及能量与反应进程的关系如图所示。下列说法正确的是( )


A.①、②、③三步反应均释放能量
B.该反应进程中有两个过渡态
C.第③步反应原子利用率为100%
D.总反应速率由第①步反应决定
【答案】D
【解析】
根据过渡态理论,反应物转化为生成物的过程中要经过能量较高的过渡态,过渡态的平均能量与反应分子的平均能量之差为反应的活化能,活化能越大,反应速率越慢,决定总反应的反应速率;反应过程是能量的变化,取决于反应物和生成物总能量的大小,生成物的总能量低于反应总能量的反应,是放热反应,若是吸热反应则相反。
A. 由能量变化关系图知第①步是吸热反应,故A错误;
B. 根据过渡态理论,反应物转化为生成物的过程中要经过能量较高的过渡态,由图可知,该反应进程中有三个过渡态,故B错误;
C. 由反应机理知,第③步反应还有H+产生,原子利用率不是100%,故C错误;
D. 总反应速率由活化能最大的那步反应即第①步反应决定,故D正确;
故选D。

【题目】铁及碳的化合物在社会生产、生活中有着广泛的应用。请回答下列问题:
(1)磁铁矿是工业上冶炼铁的原料之一。
已知:①Fe3O4(s)+4C(s)![]() 3Fe(s)+4CO(g) △H=+646.0kJmol﹣1
3Fe(s)+4CO(g) △H=+646.0kJmol﹣1
②C(s)+CO2(g)2CO(g) △H=+172.5kJmol﹣1
则Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g)△H=___。
3Fe(s)+4CO2(g)△H=___。
(2)反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)△H的平衡常数为K,在不同温度下,K值如下:
FeO(s)+CO(g)△H的平衡常数为K,在不同温度下,K值如下:
温度/K | 973 | 1173 | 1373 | 1573 |
K | 1.47 | 2.15 | 3.36 | 8.92 |
①从表中数据可推断,该反应是___(填“放热”或“吸热”)反应。
②温度为973K时,在某恒容密闭容器中发生上述反应。下列有关说法能说明该反应已达到平衡状态的是___(填字母)。
A.c(CO2)=c(CO)
B.v正(CO2)=v逆(CO)
C.体系压强不变
D.混合气体中c(CO)不变
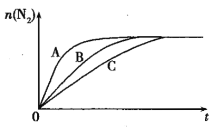
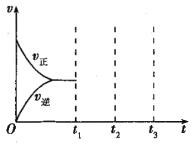
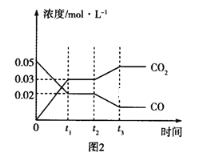
(3)如图图1、2表示反应:H2(g)+CO2(g)![]() CO(g)+H2O(g)△H>0有关量与反应时间之间的关系:
CO(g)+H2O(g)△H>0有关量与反应时间之间的关系:
①图2中若t1=0.5min,则0~t1时间段内,H2O的平均反应速率v(H2O)=___molL﹣1s﹣1。
②图1中t2时刻改变的条件是___(任写两种,下同);图2中t2时刻改变的条件是___。

【题目】盐酸和氢氧化钠是工业上重要的化工原料,也是实验室里常见的化学试剂。欲测定某NaOH溶液的物质的量浓度,可用0.1000 mol·L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为_____。
(2)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是_________。
(3)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为_____。

乙学生做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol·L-1HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.11 | 25.10 |
2 | 25.00 | 1.56 | 33.30 |
3 | 25.00 | 0.21 | 25.22 |
(4)选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为______(保留四位有效数字)。
(5)下列哪些操作会使测定结果偏高_____ (填序号)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
(6)滴定达到终点的标志是________。