题目内容
将含有2.05 g某高价含氧酸的钙盐的溶液A与含1.20 g碳酸盐的溶液B混合,恰好完全反应,生成1.25 g白色沉淀C。将滤去沉淀C的滤液蒸发,得到白色固体D,继续加热D时,D分解只得两种气态物质的混合物,在0 ℃、1×105 Pa下,体积变为0.56 L,并得到0.90 g液态水,另一种气态物质为气态氧化物R2O。试回答:
(1)白色沉淀C的物质的量为________mol。
(2)A的摩尔质量为__________,B的摩尔质量为__________。
(3)R2O与H2O的物质的量之比为__________,生成D的质量为________,D的摩尔质量为________,R2O的相对分子质量为________,R2O的化学式是____________。
(4)写出A和B混合的化学方程式_____________________________________________。
解析:由A+B===C+D知,C为CaCO3,D是一种含三 种元素的含氧酸盐,该盐只能是NH4NO3,分解生成的R2O为N2O。A为Ca(NO3)2,B为(NH4)2CO3。
种元素的含氧酸盐,该盐只能是NH4NO3,分解生成的R2O为N2O。A为Ca(NO3)2,B为(NH4)2CO3。
(1)C的物质的量为1.25 g÷100 g·mol-1=0.012 5 mol。
(2)A、B的摩尔质量分别为164 g·mol-1和96 g·mol-1。
(3)N2O的物质的量为0.56 L÷22.4 L·mol-1=0.025 mol, N2O与H2O的物质的量之比为1∶2。
答案:(1)0.012 5 (2)164 g·mol-1 96 g·mol-1
(3)1∶2 2 g 80 g·mol-1 44 N2O
(4)Ca(NO3)2+(NH4)2CO3===CaCO3↓+2NH4NO3

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目

 关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
关物理量的描述正确的是(NA表示阿伏加德罗常数)( ) 数目为0.005NA
数目为0.005NA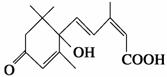 S-诱抗素制剂是一种盆栽鲜花施用剂,以保证鲜花盛开。S-诱抗素的分子结构简式如图所示,下列关于该分子的说法正确的是
S-诱抗素制剂是一种盆栽鲜花施用剂,以保证鲜花盛开。S-诱抗素的分子结构简式如图所示,下列关于该分子的说法正确的是 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-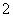 +4NH
+4NH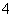 +2H2O
+2H2O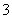 +Ba2++2OH-===BaCO3↓+2H2O+CO
+Ba2++2OH-===BaCO3↓+2H2O+CO [来源:
[来源: