题目内容
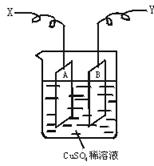
用质量均为100 g的铜作电极,电解AgNO3溶液,电解一段时间后,两极质量相差28 g,此时阳极质量为( )
| A.121.6 g | B.86 g | C.93.6 g | D.89.6 g |
C
阴极:2Ag++2e-====2Ag,阳极:Cu2++2e-====Cu
64 g·mol-1 n(Cu)+108 g·mol-1 n(Ag)="28" g(阳极减少的铜与阴极增加的银共28g)
n(Cu)=2n(Ag)(阴、阳两极转移的电子数相等)
解得n(Cu)="0.1" mol n(Ag)="0.2" mol
则阳极质量为100 g-0.1 mol×64 g·mol-1="93.6" g
64 g·mol-1 n(Cu)+108 g·mol-1 n(Ag)="28" g(阳极减少的铜与阴极增加的银共28g)
n(Cu)=2n(Ag)(阴、阳两极转移的电子数相等)
解得n(Cu)="0.1" mol n(Ag)="0.2" mol
则阳极质量为100 g-0.1 mol×64 g·mol-1="93.6" g

练习册系列答案
相关题目
 Cu
Cu