题目内容
【题目】分析城市空气样本,主要污染物为可吸入颗粒物pm2.5、SO2、NOx等,其主要来源为燃煤和机动车尾气排放等.
某同学为检测样本中所含成份,将样本用蒸馏水处理制成待测试样,设计实验及实验现象如下: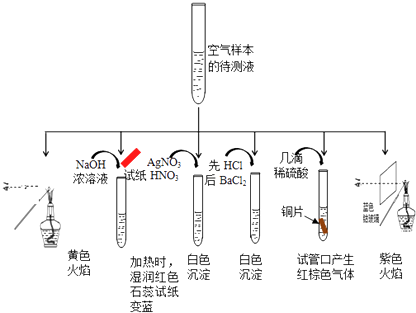
①该实验能确认存在的阳离子是 .
②该实验检测出样本中有NO3﹣ , 根据是(用化学方程式解释) .
③根据该实验能否确定样本中含有SO32﹣ , (填“能”或“否”),若要确定SO32﹣ , 所需的实验药品可以是 .
【答案】Na+、NH4+、K+;3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,2NO+O2=2NO2;否;酸性高锰酸钾溶液
【解析】解:①物质焰色反应为黄色,所以含有钠离子,和强碱共热反应产生氨气,能使石蕊试纸变蓝,证明含有铵根离子,加入硝酸酸化的硝酸银会产生白色沉淀,证明含有氯离子或是亚硫酸根离子中的一种,先加盐酸再加入氯化钡,产生白色沉淀,证明含有硫酸根离子,溶液中加入几滴硫酸,再加入金属铜,可以产生红棕色的气体,证明原溶液含有硝酸根离子,透过钴玻璃观察焰色反应呈现紫色,证明含钾离子,一定含有的钾离子是Na+、NH4+、K+ , 所以答案是:Na+、NH4+、K+;
②溶液中加入几滴硫酸,再加入金属铜,可以产生红棕色的气体,证明原溶液含有硝酸根离子,金属铜可以和硝酸反应产生硝酸铜、一氧化氮和水,一氧化氮遇到空气迅速变为红棕色,即:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,2NO+O2=2NO2 , 所以答案是:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,2NO+O2=2NO2;
③根据该实验不能确定样本中含有SO32﹣ , 加入硝酸酸化的硝酸银会产生白色沉淀,证明可能含有氯离子或是亚硫酸根离子中的一种,亚硫酸根离子可以和硝酸之间反应得到硫酸根离子,亚硫酸根离子可以使高锰酸钾褪色,但是硫酸根离子不能,可以采用高锰酸钾检验亚硫酸根离子的存在,所以答案是:否;酸性高锰酸钾溶液.

 高中必刷题系列答案
高中必刷题系列答案【题目】分析下表中各项的排布规律,按此规律排布第26项应为( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C2H4 | C2H6 | C2H6O | C2H6O2 | C3H6 | C3H8 | C3H8O | C3H8O2 | C4H8 | C4H10 |
A.C7H16
B.C7H14O2
C.C8H18
D.C8H18O
【题目】CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2 , 在催化剂的作用下发生反应:CO(g)+Cl2(g)COCl2(g)△H=a kJ/mol
反应过程中测定的部分数据如下表:
t/min | n (CO)/mol | n (Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
(1)反应0~2min末的平均速率v(COCl2)=mol/(Lmin).
(2)在2min~4min间,v(Cl2)正v(Cl2)逆 (填“>”、“=”或“<”),该温度下K= .
(3)在图1中画出0~4min末n(COCl2)随时间的变化示意图 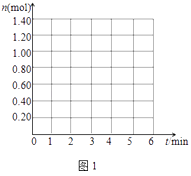
(4)已知X、L可分别代表温度或压强,如图2表示L一定时,CO的转化率随X的变化关系.X代表的物理量是;a0 (填“>”,“=”,“<”),依据是 
