题目内容
(9分)金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和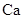 ,并含有3.5%(质量分数)
,并含有3.5%(质量分数)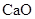 。
。
(1)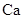 元素在周期表中位置是 ,其原子结构示意图 ;
元素在周期表中位置是 ,其原子结构示意图 ;
(2)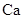 与最活跃的非金属元素A形成化合物D,D的电子式为 ;
与最活跃的非金属元素A形成化合物D,D的电子式为 ;
(3)配平用钙线氧脱鳞的化学方程式:
P + FeO + CaO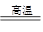 Ca3(PO4)2 + Fe;
Ca3(PO4)2 + Fe;
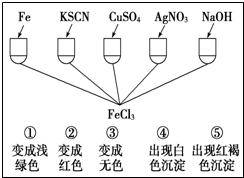
(4)将钙线试样溶于稀盐酸,加入过量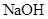 溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测
溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测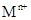 的方法是 (用离子方程式表达);
的方法是 (用离子方程式表达);
(5)取1.6g钙线试样,与水充分反映,生成224ml.H2(标准状况),在向溶液中通入适量的CO2,最多能得到CaCO3 g。
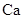 ,并含有3.5%(质量分数)
,并含有3.5%(质量分数)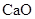 。
。(1)
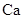 元素在周期表中位置是 ,其原子结构示意图 ;
元素在周期表中位置是 ,其原子结构示意图 ;(2)
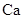 与最活跃的非金属元素A形成化合物D,D的电子式为 ;
与最活跃的非金属元素A形成化合物D,D的电子式为 ;(3)配平用钙线氧脱鳞的化学方程式:
P + FeO + CaO
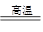 Ca3(PO4)2 + Fe;
Ca3(PO4)2 + Fe;(4)将钙线试样溶于稀盐酸,加入过量
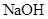 溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测
溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,则检测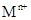 的方法是 (用离子方程式表达);
的方法是 (用离子方程式表达);(5)取1.6g钙线试样,与水充分反映,生成224ml.H2(标准状况),在向溶液中通入适量的CO2,最多能得到CaCO3 g。
(1)第四周期第ⅡA族,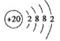 (2)
(2)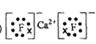
(3)2P + 5FeO + 3CaO Ca3(PO4)2+5Fe
Ca3(PO4)2+5Fe
(4)Fe3+ + 3SCN-="=" Fe(SCN)3
(5)1.1 (各2分)
 (2)
(2)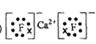
(3)2P + 5FeO + 3CaO
 Ca3(PO4)2+5Fe
Ca3(PO4)2+5Fe(4)Fe3+ + 3SCN-="=" Fe(SCN)3
(5)1.1 (各2分)
最活泼的非金属是F,即A的化学式为CaCl2,含有离子键,属于离子化合物。由方程式可知P的化合价升高5个单位,铁的化合价降低2个单位,根据得失电子守恒可以配平。白色絮状沉淀并迅速变成灰绿色,最后变成红褐色M(OH)n,说明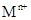 是铁离子,可用KSCN检验。1.6g钙线试样含有氧化钙
是铁离子,可用KSCN检验。1.6g钙线试样含有氧化钙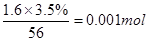 。生成224ml.H2(标准状况),因此金属钙的物质的量是
。生成224ml.H2(标准状况),因此金属钙的物质的量是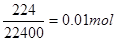 ,即最后溶液含有0.011mol钙离子,所以最终的碳酸钙沉淀是0.011mo×100g/mol=1.1g。
,即最后溶液含有0.011mol钙离子,所以最终的碳酸钙沉淀是0.011mo×100g/mol=1.1g。
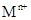 是铁离子,可用KSCN检验。1.6g钙线试样含有氧化钙
是铁离子,可用KSCN检验。1.6g钙线试样含有氧化钙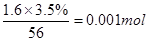 。生成224ml.H2(标准状况),因此金属钙的物质的量是
。生成224ml.H2(标准状况),因此金属钙的物质的量是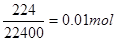 ,即最后溶液含有0.011mol钙离子,所以最终的碳酸钙沉淀是0.011mo×100g/mol=1.1g。
,即最后溶液含有0.011mol钙离子,所以最终的碳酸钙沉淀是0.011mo×100g/mol=1.1g。
练习册系列答案
相关题目

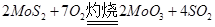 ,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为________。
,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为________。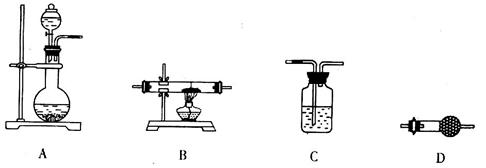
 盐酸反应)、
盐酸反应)、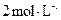 盐酸、5%NaOH溶液、饱和
盐酸、5%NaOH溶液、饱和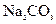 溶液、饱和
溶液、饱和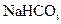 溶液和蒸馏水。
溶液和蒸馏水。
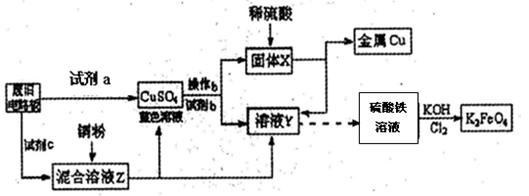
 面在同一水平面上,最后读数时右管的液面高于左管的液面,应进行的操作是
面在同一水平面上,最后读数时右管的液面高于左管的液面,应进行的操作是  。
。
 3Zn(OH)2+2Fe(OH)3+4KOH,电池工作时在正极放电的物质是: 。
3Zn(OH)2+2Fe(OH)3+4KOH,电池工作时在正极放电的物质是: 。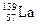 )组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x= 。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为:
)组成的一种合金LaNix是较好的储氢材料,能快速可逆地存储和释放H2。LaNix的晶胞如图,其储氢原理为:镧镍合金吸附H2,H2解离为原子,H储存在其中形成LaNixH6。LaNixH6中,x= 。该贮氢的镧镍合金、泡沫氧化镍、氢氧化钾溶液组成的镍氢电池被用于制作原子钟,反应原理为: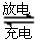 LaNix+y NiO+y H2O。写出其放电时负极的电极反应方程式
LaNix+y NiO+y H2O。写出其放电时负极的电极反应方程式 
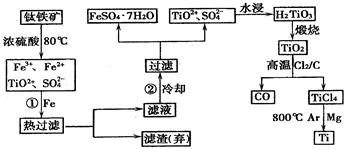
 2MgCl2+Ti , 在Ar气体中进行的目的是
2MgCl2+Ti , 在Ar气体中进行的目的是