题目内容
(1)①化合物DY2 和 DW2 的分子空间构型相似,DW2的结构式为
| D | ||||
| W | ||||
③已知aX、bY、cZ三种元素,a+b+c=26,Z的最高价氧化物的水化物与其氢化物反应生成的化合物水溶液的PH
(2)化合物XZ3是合成抗禽流感药物“达菲”的中间活性物质,XZ3 受撞击会生成一种非金属单质和一种离子化合物X3Z,请写出该反应的化学方程式
(3)化合物A、B均由上述G、W、E、X、Y五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为
②X、W、E三元素位于同一周期,且原子序数依次增大,所以E为Cl,元素W和E的最外层电子数之和与Y和X的最外层电子数之和相差6,则X的最外层电子数为1,所以X为Na;H、S、Na、O四种元素形成的能发生反应的离子化合物为NaHSO3、NaHSO4,由此写出反应的离子方程式;
③X为Na,Y为O,所以a=11,b=8,b=26-11-8=7,Z元素的质子数为7,所以Z为N元素;N的最高价氧化物的水化物为硝酸,氢化物为氨气,硝酸和氨气反应生成硝酸铵,为强酸弱碱盐,铵根离子水解,溶液显酸性,pH<7,升高温度,水解程度增强,c(H+)增大,pH减小;
(2)XZ3是NaN3,受撞击会生成非金属单质N2和离子化合物Na3N,化学方程式为3NaN3═4N2+Na3N,生成1molN2转移
| 2 |
| 3 |
(3)化合物A、B由H、S、Cl、Na、O五种元素的任意三种元素组成的强电解质,组成元素的原子数目之比均为1:1:1,若A能抑制水的电离,说明A为强碱NaOH,B能促进水的电离,两种物质水溶液的酸碱性相同,说明B为NaClO.
②X、W、E三元素位于同一周期的主族元素,且原子序数依次增大,所以E为Cl,元素W和E的最外层电子数之和与Y和X的最外层电子数之和相差6,S的最外层电子数为6,Cl的最外层电子数为7,设X的最外层电子数为x,6+x=6+7-6,x=1,X为第三周期第一主族元素Na;H、S、Na、O四种元素形成的能发生反应的离子化合物为NaHSO3、NaHSO4,NaHSO3和NaHSO4反应生成硫酸钠、二氧化硫和水,离子方程式为:HSO3-+H+=SO2↑+H2O;
③X为Na,Y为O,所以a=11,b=8,b=26-11-8=7,Z元素的质子数为7,所以Z为N元素;N的最高价氧化物的水化物为硝酸,氢化物为氨气,硝酸和氨气反应生成硝酸铵,为强酸弱碱盐,铵根离子水解,水解方程式为:NH4++H2O═NH3?H2O+H+,溶液呈酸性,pH<7;水解过程为吸热过程,给溶液加热,水解程度增强,c(H+)增大,pH减小;
(2)XZ3是NaN3,受撞击会生成非金属单质N2和离子化合物Na3N,化学方程式为3NaN3═4N2+Na3N,
由方程式可知:生成1molN2转移
| 2 |
| 3 |
标准状况下3.36L气体单质的物质的量=
| 3.36L |
| 22.4L?mol-1 |
转移电子的物质的量=0.15mol×
| 2 |
| 3 |
(3)化合物A、B由H、S、Cl、Na、O五种元素的任意三种元素组成的强电解质,组成元素的原子数目之比均为1:1:1,若A能抑制水的电离,说明A为强碱,则A为NaOH;B能促进水的电离,两种物质水溶液的酸碱性相同,而A溶液呈碱性,说明B为弱酸强碱盐NaClO.
故答案为:
(1)①S=C=S;
②HSO3-+H+═SO2↑+H2O;
③小于;减小;升高温度,水解增强,c(H+)增大;
(2)3 NaN3═4N2+Na3N;0.1 mol;
(3)NaOH;NaClO.

(16分)下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:
(除特别注明外,其它一律用化学式表示)
| A |
|
| |||||||||||||||
|
|
|
|
| W | T | M |
|
| |||||||||
| B | D |
| Z | J | L | U | V | R | |||||||||
| X | E |
|
|
|
|
| Y |
|
| G |
|
|
|
|
| Q |
|
(1)化学性质最不活泼的单质是 ,金属氢氧化物中碱性最强的是 ,
属于过渡元素的是 (填字母),J在周期表中的位置 。
(2)A 分别和L、M、T形成的化合物稳定性强弱顺序 > > ,
L、U、V的最高价氧化物对应水化物的酸性强弱顺序 > > 。
(3)V、Q形成的简单阴离子还原性强弱顺序 > ,
D、M、U、V形成的简单离子半径大小顺序 > > > 。
(4)写出Z、B分别形成的最高价氧化物对应水化物相互反应的离子方程式:
。
(5)已知G为常见的红色金属单质,现取7.68g G和50 mL 的浓硝酸反应,当G反应完毕时,溶液体积基本不变,共收集到气体的体积是3.36 L(标准状况,不考虑N2O4),剩余溶液中c(H+)= 2.2 mol/L,则原硝酸溶液的浓度为 。
(16分)下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:
(除特别注明外,其它一律用化学式表示)
|
A |
|
|
|||||||||||||||
|
|
|
|
|
W |
T |
M |
|
|
|||||||||
|
B |
D |
|
Z |
J |
L |
U |
V |
R |
|||||||||
|
X |
E |
|
|
|
|
|
Y |
|
|
G |
|
|
|
|
|
Q |
|
(1)化学性质最不活泼的单质是 ,金属氢氧化物中碱性最强的是 ,
属于过渡元素的是 (填字母),J在周期表中的位置 。
(2)A 分别和L、M、T形成的化合物稳定性强弱顺序 > > ,
L、U、V的最高价氧化物对应水化物的酸性强弱顺序 > > 。
(3)V、Q形成的简单阴离子还原性强弱顺序 > ,
D、M、U、V形成的简单离子半径大小顺序 > > > 。
(4)写出Z、B分别形成的最高价氧化物对应水化物相互反应的离子方程式:
。
(5)已知G为常见的红色金属单质,现取7.68g G和50 mL 的浓硝酸反应,当G反应完毕时,溶液体积基本不变,共收集到气体的体积是3.36 L(标准状况,不考虑N2O4),剩余溶液中c(H+)= 2.2 mol/L,则原硝酸溶液的浓度为 。
(1)①化合物DY2 和 DW2 的分子空间构型相似,DW2的结构式为______.
| D | ||||
| W | ||||
③已知aX、bY、cZ三种元素,a+b+c=26,Z的最高价氧化物的水化物与其氢化物反应生成的化合物水溶液的PH______7(填“大于”、“等于”、或“小于”);如果给溶液加热,溶液的PH______(填“增大”、“等于”、或“减小”);其变化的原因是______.
(2)化合物XZ3是合成抗禽流感药物“达菲”的中间活性物质,XZ3 受撞击会生成一种非金属单质和一种离子化合物X3Z,请写出该反应的化学方程式______.若反应生成标准状况下3.36L气体单质,则电子转移的物质的量为______.
(3)化合物A、B均由上述G、W、E、X、Y五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为______,B的化学式为______.
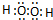
 HO2-+H+
HO2-+H+