题目内容
【题目】A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是________(填具体离子符号);由A、B、C三种元素按4∶2∶3组成的化合物所含的化学键类型属于_____。固体物质M由A和B以原子个数五比一组成的,所有原子的最外层都符合相应的稀有气体原子的最外层电子结构。该物质适当加热就分解成两种气体。则M 电子式为______,受热分解所得气体化学式是_______和_________。
(2)地壳中含量最高的金属元素的单质与D的最高价氧化物对应水化物的溶液反应,其离子方程式为____________________________。
(3)A、C两元素的单质与熔融K2CO3组成的燃料电池,其负极反应式为_______。
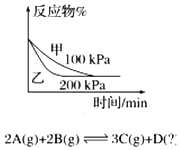
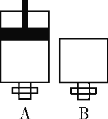
(4)可逆反应2EC2(气)+C2(气)![]() 2EC3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B容器可保持恒容(如图所示),若在A、B中分别充入1 mol C2和2 mol EC2,使反应开始时的体积V(A)=V(B),在相同温度下反应,则达平衡所需时间:t(A)__________t(B)(填“>”、“<”、“=”或“无法确定”)。
2EC3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B容器可保持恒容(如图所示),若在A、B中分别充入1 mol C2和2 mol EC2,使反应开始时的体积V(A)=V(B),在相同温度下反应,则达平衡所需时间:t(A)__________t(B)(填“>”、“<”、“=”或“无法确定”)。
【答案】 S2->O2->Na+ 共价键和离子键  NH3 H2 2Al+2OH-+2H2O=2AlO2-+3H2↑ H2-2e-+CO32-=CO2+H2O <
NH3 H2 2Al+2OH-+2H2O=2AlO2-+3H2↑ H2-2e-+CO32-=CO2+H2O <
【解析】A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和C可形成两种常见的液态化合物,则A为H元素、C为O元素,二者形成的液态化合物为H2O、H2O2,A和D最外层电子数相同,二者同主族,结合原子序数可知,D为Na;B、C和E在周期表中相邻,且C、E同主族,B、C的最外层电子数之和等于D的原子核外电子数,则B、C最外层电子数分别为5、6,可推知B为N元素、C为O元素、E为S元素,据此解答。
根据以上分析可知A为H,B为N,C为O,D为Na,E为S。则
(1)电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->O2->Na+;由H、N、O三种元素按4∶2∶3组成的化合物为NH4NO3,含有离子键、共价键。固体物质M由A和B以原子个数五比一组成的,所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,因此该物质是氢化铵,化学式为NH4H,电子式为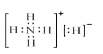 。该物质适当加热就分解成两种气体,根据原子守恒可知气体是氢气和氨气,化学式分别是NH3、H2。
。该物质适当加热就分解成两种气体,根据原子守恒可知气体是氢气和氨气,化学式分别是NH3、H2。
(2)地壳中含量最高的金属元素是铝,其单质与D的最高价氧化物对应水化物氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑。
(3)氢气、氧气与熔融K2CO3组成的燃料电池,氢气在负极放电,在熔融碳酸钾条件下生成二氧化碳与水,负极反应式为H2-2e-+CO32-=CO2+H2O;
(4)可逆反应2SO2(气)+O2(气)![]() 2SO3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,即保持恒压,B容器可保持恒容(如图所示),若在A、B中分别充入1 mol氧气和2 molSO2,使反应开始时的体积V(A)=V(B),在相同温度下反应。A中压强不变,由于正反应体积减小,因此B中压强减小,故A反应速率更快,达平衡所需时间更短,即t(A)<t(B)。
2SO3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,即保持恒压,B容器可保持恒容(如图所示),若在A、B中分别充入1 mol氧气和2 molSO2,使反应开始时的体积V(A)=V(B),在相同温度下反应。A中压强不变,由于正反应体积减小,因此B中压强减小,故A反应速率更快,达平衡所需时间更短,即t(A)<t(B)。