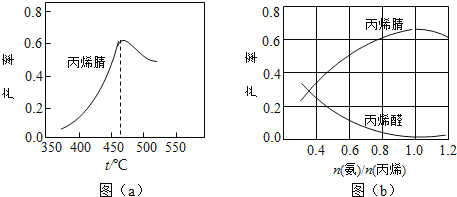
��Ŀ����
����Ŀ��ʵ���������ô�����KCl���壬��Ŀǰֻ�к�K2SO4����NH4��2CO3���ʵ�KCl��ijѧ���������ͼ��ʾ���������ᴿ��
��֪��1����NH4��2CO3![]() 2NH3��+CO2��+H2O
2NH3��+CO2��+H2O
2��K2SO4��KCl���ȶ��Ժã�KCl�ܽ�����¶ȱ仯����
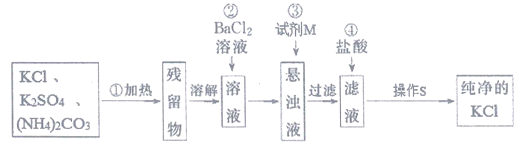
����������Ϣ���ش��������⣺
��1�����������ȵ�Ŀ���ǣ�______________���˲�����ѡ����______________���������������н��У�
��2���������������ᱵ��Һ����������_________________��
��3�����в�����ʱ�������ж�SO42-�Ƿ������ʵ�����������ͽ��ۣ�____________��
��4�������������Լ�MΪ��_______________����Ŀ����_________________��
��5������S��������__________________��
���𰸡�
��1����ȥ��NH4��2CO3���ʣ�������
��2����Һ�������µ���������NO3-��
��3��ȡ������������ϲ���Һ�еμ�BaCl2��Һ�����ް�ɫ����������˵��SO42-�ѳ�����
��4��K2CO3��Һ����ȥ����������Ĺ���Ba2+��
��5�������ᾧ��
��������
�����������1���������У�����ʱ��NH4��2CO3���ȷֽ⣬���Խ�̼��麟�ȥ�������������������н��У��ʴ�Ϊ����ȥ��NH4��2CO3���ʣ�������
��2���������������ᱵ��Һ���Ƿ�ֹ�����µ���������NO3-���ʴ�Ϊ����ֹ��Һ�������µ���������NO3-��
��3��ȡ������������ϲ���Һ�еμ�BaCl2��Һ�����ް�ɫ����������˵��SO42-�ѳ������ʴ�Ϊ��ȡ������������ϲ���Һ�еμ�BaCl2��Һ�����ް�ɫ����������˵��SO42-�ѳ�����
��4����������Ŀ���dz�ȥ�������Ȼ�����Һ������ѡ��̼��أ��γ�̼�ᱵ�������ʴ�Ϊ��K2CO3��Һ����ȥ����������Ĺ���Ba2+��
��5������S�Ǵ��Ȼ�����Һ�л���Ȼ��ؾ��壬����ͨ�������ᾧ�ķ������У��ʴ�Ϊ�������ᾧ��

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�