题目内容
12.(1)写出下列物质的电子式:甲基
 NaCl
NaCl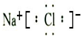 H2O2
H2O2
(2)写出下列物质的名称
 2,3,5-三甲基己烷;
2,3,5-三甲基己烷;  2,4-二甲基己烷.
2,4-二甲基己烷.
分析 (1)甲基中含有3个碳氢键,碳原子最外层为7个电子,据此写出甲基的电子式;
氯化钠为离子化合物,钠离子与氯离子通过离子键结合;
过氧化氢为共价化合物,两个氧原子之间共用1对电子,两个氢原子分别与1个氧原子共用1对电子;
(2)根据烷烃烷烃命名原则完成:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
解答 解:(1)甲基中含有3个碳氢键,碳原子最外层为7个电子,电子式为: ;
;
故答案为: ;
;
氯化钠为离子化合物,钠离子与氯离子通过离子键结合,电子式为: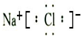 ;
;
故答案为: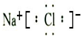 ;
;
过氧化氢为共价化合物,两个氧原子之间共用1对电子,两个氢原子分别与1个氧原子共用1对电子,电子式为: ;
;
故答案为: ;
;
(2) 为烷烃,主链上有6个C,2,3,5号碳上各有1个甲基,系统命名为:2,3,5-三甲基己烷;
为烷烃,主链上有6个C,2,3,5号碳上各有1个甲基,系统命名为:2,3,5-三甲基己烷;
故答案为:2,3,5-三甲基己烷; 为烷烃,主链上有6个碳原子,3,4号碳上各有1个甲基,系统命名为:2,4-二甲基己烷;
为烷烃,主链上有6个碳原子,3,4号碳上各有1个甲基,系统命名为:2,4-二甲基己烷;
故答案为:2,4-二甲基己烷;
点评 本题考查了电子式的书写、有机物系统命名,书写物质所含化学键类型是解题关键,注意烷烃系统命名的规则,题目难度不大.

练习册系列答案
相关题目
17.下列微粒中:①12Mg2+ ②Na2-③ ④O2-,核外电子总数相同的是( )
④O2-,核外电子总数相同的是( )
 ④O2-,核外电子总数相同的是( )
④O2-,核外电子总数相同的是( )| A. | ②③④ | B. | ①②④ | C. | ①②③ | D. | ①③④ |
20.下列过程不发生化学变化的是( )
| A. | 石油的分馏 | B. | 煤的干馏 | ||
| C. | 以海水为原料获取单质溴 | D. | 蛋白质溶液中滴加硫酸铜 |
7.下列反应能说明乙烯具有不饱键的是( )
| A. | 燃烧反应 | B. | 取代反应 | C. | 硝化反应 | D. | 加成反应 |
4.下列说法不正确的是( )
| A. | 石油的催化重整是为了获得以汽油为主的轻质油 | |
| B. | 芳香烃主要来自于煤干馏后的煤焦油 | |
| C. | 汽油、煤油、柴油主要来自于石油的常压蒸馏 | |
| D. | 乙烯可由石油裂解得到 |
1. 请回答下列问题:
请回答下列问题:
(1)下表列出了一些化学键的键能E:
反应H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,则x=496.4.
(2)铅蓄电池是正极板上覆盖有PbO2,负极板上覆盖有Pb,电解质溶液是H2SO4溶液,电池放电时的总反应:Pb+PbO2+2H2SO4═2PbSO4+2H2O.
请写出充电时阴极的电极反应式:PbSO4+2e-═Pb+SO42-
(3)反应m A+n B?p C,在某温度下达到平衡.
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是m+n>p.
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向逆反应方向移动.
③若再升高温度,平衡向逆向移动,则正反应为放热反应(填“吸热”或“放热”)
(4)依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.
①请在图中标出电极材料及电解质溶液(写化学式)
②盐桥中的Cl-向左极移动(填“左”或“右”).
 请回答下列问题:
请回答下列问题:(1)下表列出了一些化学键的键能E:
| 化学键 | H-H | O═O | O-H |
| E/kJ•mol-1 | 436 | x | 463 |
(2)铅蓄电池是正极板上覆盖有PbO2,负极板上覆盖有Pb,电解质溶液是H2SO4溶液,电池放电时的总反应:Pb+PbO2+2H2SO4═2PbSO4+2H2O.
请写出充电时阴极的电极反应式:PbSO4+2e-═Pb+SO42-
(3)反应m A+n B?p C,在某温度下达到平衡.
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是m+n>p.
②若C为气体,且m+n=p,在加压时化学平衡发生移动,则平衡必定向逆反应方向移动.
③若再升高温度,平衡向逆向移动,则正反应为放热反应(填“吸热”或“放热”)
(4)依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.
①请在图中标出电极材料及电解质溶液(写化学式)
②盐桥中的Cl-向左极移动(填“左”或“右”).
 材料是人类赖以生存和发展的重要物质基础.
材料是人类赖以生存和发展的重要物质基础.


 .
. .
. .
.