��Ŀ����
����Ŀ��ƻ������һ�ֳ������л�������ṹ��ʽΪ![]() ��
��
��1��ƻ������������������ŵ�������_______________��
��2��ƻ������ܷ����ķ�Ӧ��________(�����)��
�ټӳɷ�Ӧ ��������Ӧ �ۼӾ۷�Ӧ ��������Ӧ ����ȥ��Ӧ ��ȡ����Ӧ
��3������A 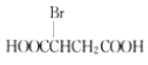 �����Ҷ�����Ӧ���ɰ�Ԫ��������д���˹��̵Ļ�ѧ����ʽ��______________________________________________��
�����Ҷ�����Ӧ���ɰ�Ԫ��������д���˹��̵Ļ�ѧ����ʽ��______________________________________________��
��4��д��ƻ������Ũ��������������ᷴӦ�Ļ�ѧ����ʽ_______________________����Ӧ����Ϊ_________________
���𰸡� �ǻ��� �Ȼ� �٢� 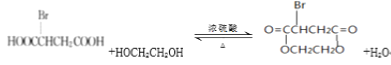
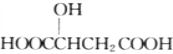 +CH3COOH
+CH3COOH ![]() CH3COO-CH(COOH)-CH2COOH + H2O ������Ӧ��ȡ����Ӧ��
CH3COO-CH(COOH)-CH2COOH + H2O ������Ӧ��ȡ����Ӧ��
�������������������1������ƻ����Ľṹ��ʽ![]() �������к���-OH��-COOH��
���������-OH��-COOH��
��2������ƻ��������к���-OH��-COOH�����ŷ�����
��3��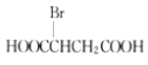 �е������Ȼ����Ҷ����е������ǻ�����������Ӧ�����ɰ�Ԫ��������4��ƻ�����е��ǻ���Ũ��������������������е��Ȼ�����������Ӧ��
�е������Ȼ����Ҷ����е������ǻ�����������Ӧ�����ɰ�Ԫ��������4��ƻ�����е��ǻ���Ũ��������������������е��Ȼ�����������Ӧ��
��������1��ƻ����Ľṹ��ʽ![]() �������к���-OH��-COOH,�������ǻ����Ȼ���
�������к���-OH��-COOH,�������ǻ����Ȼ���
��2����ƻ���������û��̼̼˫�������ܷ����ӳɷ�Ӧ�� ��ƻ��������к����Ȼ����ǻ����ܷ���������Ӧ�� ��ƻ���������û��̼̼˫�������ܷ����Ӿ۷�Ӧ�� ��ƻ��������к����ǻ����ܷ���������Ӧ�� ��ƻ��������к����ǻ����ܷ�����ȥ��Ӧ�� ��ƻ��������к����ǻ����Ȼ����ܷ���ȡ����Ӧ��ѡ�٢ۣ�
��3��![]() �е������Ȼ����Ҷ����е������ǻ�����������Ӧ�����ɰ�Ԫ��������Ӧ����ʽ��
�е������Ȼ����Ҷ����е������ǻ�����������Ӧ�����ɰ�Ԫ��������Ӧ����ʽ��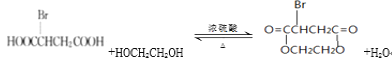 ����4��ƻ�����е��ǻ���Ũ����������������е��Ȼ�����������Ӧ����Ӧ����ʽ��
����4��ƻ�����е��ǻ���Ũ����������������е��Ȼ�����������Ӧ����Ӧ����ʽ��![]() +CH3COOH
+CH3COOH ![]() CH3COO-CH(COOH)-CH2COOH + H2O��
CH3COO-CH(COOH)-CH2COOH + H2O��

����Ŀ����������ṹ�����Ŀ��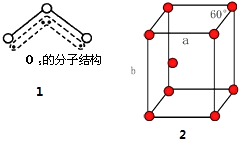
��1���ù��ʾ��ͼ��ʾFe3+�ļ۵����Ų� ��
��2��ij����Ԫ�صĵ����ܣ����ӷ��أ����£�
I1 | I2 | I3 | I4 | I5 | I6 | I7 |
14.5 | 29.6 | 47.4 | 77.5 | 97.9 | 551.9 | 666.8 |
�жϸ�Ԫ�ش����壻
��3����ABn������ԭ��A��û��δ�����γɹ��ۼ��ŶԵ��ӣ����ü۲���ӶԻ���ģ�ͣ�����˵����ȷ����������ĸ����
A.��n=2������ӵ����幹��ΪV��
B.��n=3������ӵ����幹��Ϊ������
C.��n=4������ӵ����幹��Ϊ����������
D.����˵��������ȷ
��4���������ӵĽṹ��ͼ1����V�ͣ�����116.5�㣮��ش𣺢ٳ����������Ĺ�ϵ�� ��
�����з�����������ӵĽṹ�����Ƶ���������ĸ����
A��H2O B��CO2 C��SO2 D��BeCl2
�۳��������Ƿ�Ϊ���Է�������ǡ�����
��5���ڶ�����Ԫ���У�������Ԫ����ɵļ������Ӽ����й��ۼ�����λ�����������������������������8���������ʵĵ���ʽ ��
��6��������Ϊ�������ܶѻ��ṹ������ѵ�ԭ�Ӱ뾶Ϊr�������ṹ��ͼ2��ʾ����þ����ı߳�a= �� b=���ú�r�Ĵ���ʽ��ʾ��
����Ŀ���ҹ��Ǹ������������������Ϊ�����һ����¯��������Ϊ�ձ������������
��1��I����֪��Ӧ ![]() Fe2O3��s��+CO��g��
Fe2O3��s��+CO��g�� ![]() Fe��s��+CO2��g����H=��23.5kJmol��1 �� �÷�Ӧ��1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol��Ӧ����l0min��ﵽƽ�⣮ ��CO��ƽ��ת����=
Fe��s��+CO2��g����H=��23.5kJmol��1 �� �÷�Ӧ��1000���ƽ�ⳣ������4����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol��Ӧ����l0min��ﵽƽ�⣮ ��CO��ƽ��ת����=
�������CO��ƽ��ת���ʣ��ٽ�Fe2O3��ת�����ɲ�ȡ�Ĵ�ʩ�� ��
a����߷�Ӧ�¶�
b������Ӧ��ϵ��ѹǿ
c��ѡȡ���ʵĴ���
d����ʱ���ջ��Ƴ�����CO2
e�������ʯ��ʹ����ƽ���������ֽӴ�
��2����¯���������ķ����е�CO�ɽ��л��գ�ʹ����һ�������º�H2��Ӧ�Ʊ��״���CO��g��+2H2��g��CH3OH��g���������ͼʾ�ش��������⣺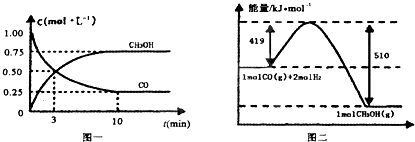
�ٴӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����v��H2��= ��
����֪������ȼ����286kJ/mol����д���״����岻���ȼ�յ��Ȼ�ѧ����ʽ ��
�������¶Ⱥ�������ͬ�������ܱ������У�����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ�ﵽƽ�ⅼ���й��������±���
���� | ��Ӧ��Ͷ����� | ��Ӧ��� | CH3OH��Ũ�� | �����仯 |
�� | 1mol CO��2mol H2 | ��1 | c1 | �ų�Q1kJ���� |
�� | 1mol CH3OH | ��2 | c2 | ����Q2kJ���� |
�� | 2mol CO��4mol H2 | ��3 | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ����
A��c1=c2B.2Q1=Q3C.2��1=��3D����1+��2=1E���÷�Ӧ������1mol CH3OH����ų���Q1+Q2��kJ������