题目内容
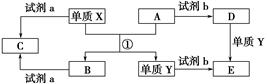
有关物质间转化关系如下图,试回答:

(1)转化①的反应条件为 .
(2)转化②的化学方程式为 .转化③的离子方程式为 .
(3)若转化⑤用于实验室制Al(OH)3,则试剂A宜选择 (填名称).
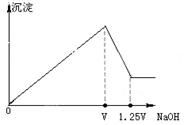
(4)向50 mL 3 mol·L-1 AlCl3溶液中滴加1 mol·L-1 NaOH溶液,结果Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为 或 mL。

(1)转化①的反应条件为 .
(2)转化②的化学方程式为 .转化③的离子方程式为 .
(3)若转化⑤用于实验室制Al(OH)3,则试剂A宜选择 (填名称).
(4)向50 mL 3 mol·L-1 AlCl3溶液中滴加1 mol·L-1 NaOH溶液,结果Al3+离子有1/3转化为Al(OH) 3沉淀,则加入的NaOH溶液的体积可能为 或 mL。
(1)电解
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑,MnO2+4H++2Cl- Cl2↑+Mn2++2H2O
Cl2↑+Mn2++2H2O
(3)氨水
(4)150ml、550ml
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑,MnO2+4H++2Cl-
 Cl2↑+Mn2++2H2O
Cl2↑+Mn2++2H2O(3)氨水
(4)150ml、550ml
试题解析:(1)由氧化铝制取铝单质,通过电解的方法。
(2)转化②是指铝和氢氧化钠溶液的反应,所以方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,转化③是指二氧化锰与浓盐酸反应制取氯气,所以离子方程式为MnO2+4H++2Cl-
 Cl2↑+Mn2++2H2O。
Cl2↑+Mn2++2H2O。(3)因为氢氧化铝易溶解于强碱溶液,所以制备氢氧化铝时常用弱碱溶液氨水。
(4)由题意可知氯化铝的物质的量为0.15mol, Al3+离子有1/3转化为Al(OH) 3时,有两种情况:一、NaOH不足,这时有0.05mol的Al(OH) 3生成则需要NaOH0.15mol,体积为150ml;二、NaOH过量时,生成0.15mol的Al(OH) 3需要0.45mol的NaOH,再溶解0.1mol的Al(OH) 3需要0.1mol的NaOH,所以共需要0.55mol的NaOH,体积为550ml。

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
 xFe2O3的铝灰制备Al2(S04)3
xFe2O3的铝灰制备Al2(S04)3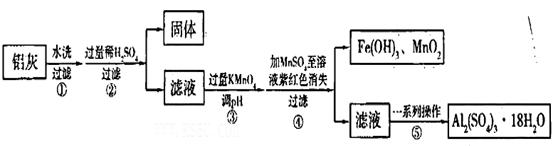

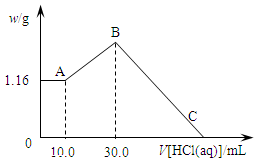
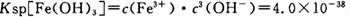 当pH=2时,Fe3+开始沉淀的浓度为_______________。
当pH=2时,Fe3+开始沉淀的浓度为_______________。