题目内容
(原创)用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,46g NO2中含有的分子数为NA |
| B.通常状况下,14g CO含有的电子数目为7NA |
| C.1L 0.2 mol/L的CH3COOH溶液中,H+ 数目为0.2NA |
| D.0.1mol Cu 和与40mL 10mol/L硝酸反应后,溶液中的NO3-数目为0.2NA |
B
解析试题分析:A、NO2气体中存在平衡:2NO2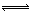 N2O4,所以标准状况下,46g NO2中含有的分子数小于NA,错误;B、14g CO物质的量为0.5mol,含有的电子数为0.5mol×14=7mol,数目为7NA,正确;C、CH3COOH是弱电解质,少量电离,所以1L 0.2 mol/L的CH3COOH溶液中,H+ 数目小于0.2NA,错误;D、反应第一阶段,Cu与浓硝酸反应,Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,随着反应的进行,浓硝酸变为稀硝酸,发生反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+2H2O,HNO3过量,所以NO3-数目大于0.2NA,错误。
N2O4,所以标准状况下,46g NO2中含有的分子数小于NA,错误;B、14g CO物质的量为0.5mol,含有的电子数为0.5mol×14=7mol,数目为7NA,正确;C、CH3COOH是弱电解质,少量电离,所以1L 0.2 mol/L的CH3COOH溶液中,H+ 数目小于0.2NA,错误;D、反应第一阶段,Cu与浓硝酸反应,Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,随着反应的进行,浓硝酸变为稀硝酸,发生反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+2H2O,HNO3过量,所以NO3-数目大于0.2NA,错误。
考点:本题考查阿伏伽德罗常数的应用。

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
下列变化属于物理变化的是 ( )
| A.氧气在放电条件下变成臭氧 |
| B.胆矾在加热条件下变成白色无水硫酸铜 |
| C.漂白的草帽久置空气中变黄 |
| D.氢氧化铁胶体加入硫酸镁产生沉淀 |
下列说法正确的是( )
| A.同温同压下,相同体积的物质,其物质的量一定相等 |
| B.标准状况下气体摩尔体积约为22.4L |
| C.0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的数目之比为15∶2 |
| D.150 mL 1 mol/L NaCl溶液与50 mL 1 mol/L AlCl3溶液中Cl-物质的量浓度相等 |
下列表示物质结构的化学用语或模型图正确的是
A.H2O2的电子式: | B.CH4的球棍模型: |
C. 的原子结构示意图: 的原子结构示意图: | D.CCl4的结构式: |
若阿伏加德罗常数的数值用NA表示,下列说法正确的是( )
| A.标准状况下,1.12L氦气所含原子数为0.1NA | B.1.6gNH2-离子所含质子数为NA |
| C.22.4 LHCl溶于水,溶液中H+数为NA | D.9g D2O所含的中子数为4.5NA |
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L,向反应后的溶液中加入c mol/L KOH溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为 n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体 p g。下列关系式中不正确的是(相对质量:Mg:24 Al:27 O:16 H:1)
| A.c=1000b/11.2V | B.p=m+Vc/125 | C.n=m+17Vc | D.5m/3<p<17m/9 |
设NA为阿伏加德罗常数的值。下列说法一定正确的是 ( )
| A.常温下,1 L 0.1 mol/L的NH4NO3溶液中氧原子数为0.3NA |
| B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA |
| C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的O原子数目为0.2NA |
| D.Fe与水蒸气在高温条件下反应,有1 mol Fe参与反应,则转移电子的数目为3NA |
下列各项化学用语中表示正确的是( )
A.Na2O2的电子式为: |
B.丙烷分子的比例模型为: |
| C.甲醛的结构简式:HCHO |
D.聚丙烯的结构简式为: |
