题目内容
为了描述方便,人们常用电子式来表示原子、分子,下列电子式书写正确的是( )
D
解析试题分析:A、N2的电子式为: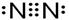 ,错误;B、不存在
,错误;B、不存在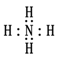 这种微粒,错误;C、H2O中H与
这种微粒,错误;C、H2O中H与
O之间形成了共价键,电子式为: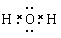 ,错误;D、NaCl中Na+与Cl?形成离子键,电子式为:
,错误;D、NaCl中Na+与Cl?形成离子键,电子式为: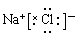 ,正确。
,正确。
考点:本题考查电子式的书写。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
A.羟基的电子式为: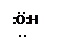 | B.HClO的结构式:H—Cl—O |
C.丙烷分子的比例模型: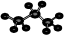 | D.S2-的结构示意图: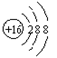 |
在下列变化中,只发生物理变化的是
| A.空气液化制取氮气 | B.酸雨侵蚀建筑物 |
| C.荔枝酿酒 | D.生石灰遇水成为熟石灰 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.0.1molCl2常温下与过量NaOH溶液反应转移电子总数为 0.1NA |
| B.25℃时, pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
| C.0.25mol Na2O2中含有的阴离子数为0.5 NA |
| D.1L0.1mol·L-1的硫化钠溶液中硫离子数目为0.1NA |
下列说法中正确的是
| A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L |
| B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L |
| C.配制500 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾 |
| D.中和100 mL 1 mol/L的H2SO4溶液,需NaOH 4 g |
下列说法正确的是
| A.将 100g10%的盐酸加热蒸发,得到 50 g溶液,其浓度为20% |
| B.把3mol/L的硫酸与等体积的水混合,所得溶液的浓度大于1.5 mol/L |
| C.把200mL3mol/L的BaCl2溶液跟100mL3mol/L的KCl溶液混合后,溶液中的c(Cl-)仍然是3 mol/L |
| D.已知某温度下KNO3的溶解度是 31.6 g/ 100 g水,在该温度下将 20 g的KNO3溶于 50 g的水中,所得溶液的质量分数是28.6% |
(原创)用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,46g NO2中含有的分子数为NA |
| B.通常状况下,14g CO含有的电子数目为7NA |
| C.1L 0.2 mol/L的CH3COOH溶液中,H+ 数目为0.2NA |
| D.0.1mol Cu 和与40mL 10mol/L硝酸反应后,溶液中的NO3-数目为0.2NA |
下列化学用语表示正确的是
| A.高氯酸的化学式:HClO3 | B.氮气的电子式: |
C.氟原子结构示意图: | D.乙烯的结构简式:CH2CH2 |