题目内容
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层 只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是 ,A、B、C、D的第一电离能由小到大的顺序为 。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是 ;
(3)A的最高价含氧酸根离子中,其中心原子采取 杂化,D的低价氧化物分子的空间构型是 。
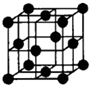
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为 ;(每个球均表示1个 原子)
(1)1s22s22p63s23p63d104s1(或[Ar] 3d104s1)(2分);
Al<Mg< S<N(1分)
(2)MgCl2为离子晶体而AlCl3为分子晶体(1分)
(3)sp2(1分),V形(1分)
(4)Cu3 N (2分)
解析:
A原子核外有三个未成对电子,则其电子排布式为:ns2np3,结合A与B可形成离子化合物B3A2,且原子序数最小,则可推出二者分别为氮元素和镁元素;C元素是地壳中含量最高的金属元素,故C为铝元素;D原子核外的M层中有两对成对电子,则其电子排布式必为:1s22s22p63s23p4,为硫元素;E原子核外最外层只有1个电子,其余各层电子均充满,且原子序数最大,为第四周期,其电子排布必为:1s22s22p63s23p63d104s1,为铜元素。

| A、Fe、Cu、Al、Ag | B、Al、Cu、Fe、Ag | C、Cu、Ag、Al、Fe | D、Ag、Al、Cu、Fe |

 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素. (Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答:
(Ⅰ)通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答: