题目内容
【题目】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
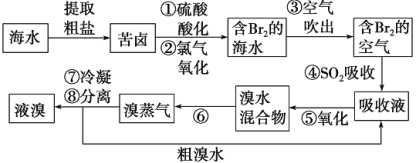
(1)步骤①中用硫酸酸化的目的是 ;
步骤②发生反应的离子方程式为 。
(2)步骤④利用了SO2的还原性,反应的离子方程式: 。
(3)步骤⑥的名称是 。
(4)从含Br2的海水中吹出的溴也可用纯碱吸收,纯碱吸收溴的主要反应是3Na2CO3+3Br2==NaBrO3+5NaBr+3CO2;吸收1 mol Br2时,转移的电子为_________mol。
【答案】
(1)酸化可抑制Cl2、Br2与水的反应;Cl2+2Br-===2Cl-+Br2
(2)Br2+2H2O+SO2=SO![]() +4H++2Br-;
+4H++2Br-;
(3)蒸馏;(4)![]()
【解析】
试题分析:(1)氯气、溴单质与水之间能发生反应,酸化可抑制它们与水的反应,氯气能将溴离子氧化为溴单质,即Cl2+2Br-=Br2+2Cl-,故答案为:酸化可抑制Cl2、Br2与水反应;Cl2+2Br-=Br2+2Cl-;
(2)SO2和氯气、水反应生成硫酸和氢溴酸,即:Br2+SO2+2H2O=4H++2Br-+SO42-,故答案为:Br2+SO2+2H2O=4H++2Br-+SO42-;
(3)溴水的混合物中,将溴单质和水分离得到溴蒸汽可以采用蒸馏法,故答案为:蒸馏;
(4)反应中Br2起氧化剂、还原剂作用,根据电子转移守恒可知,2×n氧化剂(Br2)=2×5×n还原剂(Br2),故n氧化剂(Br2):n还原剂(Br2)=5:1,故吸收1mol Br2时,转移的电子数为1mol×2×![]() ×5=
×5=![]() mol,故答案为:
mol,故答案为:![]() 。
。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目