题目内容
(2013?江西模拟)亚氯酸钠(NaClO2)是一种重要的消毒剂.已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2?3H2O,②ClO2的沸点为283K,纯ClO2易分解爆炸,③HClO2在25℃时的电离程度与硫酸的第二步电离程度相当,可视为强酸.如图是过氧化氢法生产亚氯酸钠的工艺流程图:
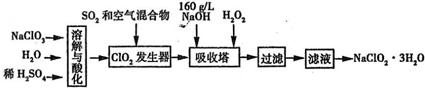
(1)C1O2发生器中所发生反应的离子方程式为
A.将SO2氧化成SO3增强酸性 B.稀释C1O2以防止爆炸 C.将NaClO3氧化成C1O2
(2)在该实验中用质量浓度来表示NaOH溶液的组成,若实验时需要450mLl60g/L的NaOH溶液,则在精确配制时,需要称取NaOH的质量是
(3)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量所需要的试剂是
(4)在吸收塔中,可代替H2O2的试剂是
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
(5)从滤液中得到NaClO2?3H2O晶体的实验操作依次是

(1)C1O2发生器中所发生反应的离子方程式为
2SO2+ClO3-=C1O2+2SO42-
2SO2+ClO3-=C1O2+2SO42-
,发生器中鼓入空气的作用可能是B
B
(选填序号).A.将SO2氧化成SO3增强酸性 B.稀释C1O2以防止爆炸 C.将NaClO3氧化成C1O2
(2)在该实验中用质量浓度来表示NaOH溶液的组成,若实验时需要450mLl60g/L的NaOH溶液,则在精确配制时,需要称取NaOH的质量是
80.0
80.0
g,所使用的仪器除托盘天平、量筒、烧杯、玻璃棒外,还必须有500ml容量瓶、胶头滴管、药匙
500ml容量瓶、胶头滴管、药匙
.(3)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量所需要的试剂是
酚酞
酚酞
.(4)在吸收塔中,可代替H2O2的试剂是
A
A
(填序号).A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
(5)从滤液中得到NaClO2?3H2O晶体的实验操作依次是
加热浓缩、冷却结晶、过滤
加热浓缩、冷却结晶、过滤
(填操作名称)分析:(1)由流程图可知C1O2发生器中目的是产生C1O2,二氧化硫具有还原性,将ClO3-还原为C1O2,自身被氧化为SO42-;
由信息②可知,纯ClO2易分解爆炸,一般用稀有气体或空气稀释,以防止爆炸;
(2)选择500mL容量瓶,浓度g/L表示1L溶液中所含溶质质量的多少,据此计算配制500mLl60g/L的NaOH溶液需要氢氧化钠的质量;
配制氢氧化钠溶液需要仪器有:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
(3)检验溶液的酸碱性可用酸碱指示剂.
(4)还原性要适中,还原性太强,会将ClO2还原为更低价态产物,影响NaClO2生产,同时方便后续分离提纯,加入试剂不能干扰后续生产,Na2O2溶于水相当于H2O2.
(5)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体.得到的粗晶体经过重结晶可得到纯度更高的晶体.
由信息②可知,纯ClO2易分解爆炸,一般用稀有气体或空气稀释,以防止爆炸;
(2)选择500mL容量瓶,浓度g/L表示1L溶液中所含溶质质量的多少,据此计算配制500mLl60g/L的NaOH溶液需要氢氧化钠的质量;
配制氢氧化钠溶液需要仪器有:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
(3)检验溶液的酸碱性可用酸碱指示剂.
(4)还原性要适中,还原性太强,会将ClO2还原为更低价态产物,影响NaClO2生产,同时方便后续分离提纯,加入试剂不能干扰后续生产,Na2O2溶于水相当于H2O2.
(5)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体.得到的粗晶体经过重结晶可得到纯度更高的晶体.
解答:解:(1)由流程图可知C1O2发生器中目的是产生C1O2,二氧化硫具有还原性,将ClO3-还原为C1O2,自身被氧化为SO42-,反应离子方程式为2SO2+ClO3-=C1O2+2SO42-;
由信息②可知,纯ClO2易分解爆炸,发生器中鼓入空气的作用应是稀释ClO2,以防止爆炸,故选B;
故答案为:2SO2+ClO3-=C1O2+2SO42-;B;
(2)应选择500mL容量瓶,浓度g/L表示1L溶液中所含溶质质量的多少,配制500mLl60g/L的NaOH溶液需要氢氧化钠的质量为0.5L×l60g/L=80.0g;
配制氢氧化钠溶液需要仪器有:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故还需要的仪器为:500ml容量瓶、胶头滴管、药匙;
故答案为:80.0;500ml容量瓶、胶头滴管、药匙;
(3)NaOH过量则溶液呈碱性,取少许溶液加入酚酞,溶液若呈红色,说明NaOH过量;
故答案为:酚酞;
(4)还原性要适中.还原性太强,会将ClO2还原为更低价态产物,影响NaClO2生产;方便后续分离提纯,加入试剂不能干扰后续生产.Na2O2溶于水相当于H2O2.Na2S、FeCl2还原性较强,生成物与NaClO2分离比较困难;
故选A;
(5)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体.得到的粗晶体经过重结晶可得到纯度更高的晶体.
故答案为:加热浓缩、冷却结晶、过滤.
由信息②可知,纯ClO2易分解爆炸,发生器中鼓入空气的作用应是稀释ClO2,以防止爆炸,故选B;
故答案为:2SO2+ClO3-=C1O2+2SO42-;B;
(2)应选择500mL容量瓶,浓度g/L表示1L溶液中所含溶质质量的多少,配制500mLl60g/L的NaOH溶液需要氢氧化钠的质量为0.5L×l60g/L=80.0g;
配制氢氧化钠溶液需要仪器有:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,故还需要的仪器为:500ml容量瓶、胶头滴管、药匙;
故答案为:80.0;500ml容量瓶、胶头滴管、药匙;
(3)NaOH过量则溶液呈碱性,取少许溶液加入酚酞,溶液若呈红色,说明NaOH过量;
故答案为:酚酞;
(4)还原性要适中.还原性太强,会将ClO2还原为更低价态产物,影响NaClO2生产;方便后续分离提纯,加入试剂不能干扰后续生产.Na2O2溶于水相当于H2O2.Na2S、FeCl2还原性较强,生成物与NaClO2分离比较困难;
故选A;
(5)从溶液中得到含结晶水的晶体,只能采取蒸发、浓缩、冷却结晶方法,通过过滤得到粗晶体.得到的粗晶体经过重结晶可得到纯度更高的晶体.
故答案为:加热浓缩、冷却结晶、过滤.
点评:本题以学生比较陌生的亚氯酸钠制备为背景,以过氧化氢法制备亚氯酸钠为主线,考察学生阅读题目获取信息的能力、对浓度概念的理解、对氧化还原反应相关知识的运用、有关实验操作和简单实验设计能力考察以及在新情境下综合运用知识解决问题的能力.题目有一定的难度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
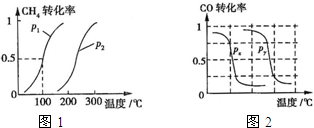 (2013?江西模拟)甲醇是一种很好的燃料,工业上用CH4和H2O为原料,通过下述反应Ⅰ和Ⅱ来制备甲醇.
(2013?江西模拟)甲醇是一种很好的燃料,工业上用CH4和H2O为原料,通过下述反应Ⅰ和Ⅱ来制备甲醇.


