题目内容
碳元素与某非金属元素R形成化合物CRx,已知CRx分子中各原子最外层电子数之和是32,核外电子数之和为74,则R是什么元素,x等于多少?并写出R元素最高价氧化物及对应水化物的化学式。
答案:
解析:
解析:
| 氯元素;4;HClO4
设非金属元素R原子最外层电子数为y,R原子核外电子数为z,则根据题意有:
因为x,y,z都是正整数,且最外层电子数不超过8个,所以R元素最外层电子数为7,R原子核外电子总数是17,R是氯元素。 根据C 所以其高价氧化物为Cl2O7,其最高氧化物对应水化物的化学式为HClO4。
|

练习册系列答案
相关题目
 与某非金属元素R形成化合物
与某非金属元素R形成化合物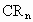 ,已知
,已知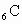 与某非金属元素R形成化合物
与某非金属元素R形成化合物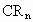 ,已知
,已知