题目内容
【题目】德国化学家哈伯(F. Haber, 1868-1930)发明的合成氨技术使大气中的氮气变成了生产氮肥的永不枯竭的廉价来源,从而使农业生产依赖土壤的程度减弱,解决了地球上因粮食不足导致的饥饿和死亡问题。因此这位解救世界粮食危机的化学天才获得了 1918年诺贝尔化学奖。现在我们在实验室模拟工业制氨的过程,以探究外界条件对平衡的影响。
查阅资料,获得以下键能数据:
化学键 | N≡N | H-H | N-H |
键能/(kJ/mol) | 946 | 436 | 391 |
(1)计算工业合成氨反应的反应热:N2(g)+3H2(g) ![]() 2NH3(g) △H=________ kJ/mol
2NH3(g) △H=________ kJ/mol
(2)一定温度下,向一个恒压容器中充入N20.6mol,H2 0 .5mol,在一定温度下进行反应:N2(g)+3H2(g) ![]() 2NH3(g),达到平衡时,N2的转化率为1/6,此时容器的体积为1L。
2NH3(g),达到平衡时,N2的转化率为1/6,此时容器的体积为1L。
①该温度时容器中平衡体系的平衡常数是______________。
②若保持平衡时的温度和压强不变,继续向平衡体系中通入0.9mol N2,则平衡将____(填“正向”,“逆向”或“不”)移动。
(3)在两个压强相等,温度分别为T1和T2的容器中充入由1 mol N2和3 molH2组成的混合气体,发生反应N2(g)+3H2(g) ![]() 2NH3(g),平衡后改变容器体积,容器内 N2的体积分数随压强的变化如图所示。据图判断下列说法正确的是______________
2NH3(g),平衡后改变容器体积,容器内 N2的体积分数随压强的变化如图所示。据图判断下列说法正确的是______________

a.A、 B、 C三点的平衡常数大小关系:KA<KB<KC
b.B点和C点的H2浓度大小关系:B<C
c.A点和B点混合气体的密度大小关系:A<B
d.A点和C点混合气体的平均相对分子质量大小关系:A>C
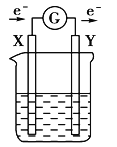
(4)合成氨工业会产生大量副产物CO2,工业上常用高浓度的K2CO3溶液吸收CO2,,得溶液X,再利用电解法K2CO3溶液再生,其装置如图所示:

①在阳极区发生的反应包括____________________和H++ HCO3-=H2O+CO2↑。
②简述CO32-在阴极区再生的原理________________。
③再生装置中产生的CO2和H2在一定条件下反应生成甲醇,工业上利用该反应合成甲醇。
已知:25 ℃,101 KPa下:
2H2(g)+ O2(g)=2H2O(g) Δ H1=-484kJ/mol
2CH3OH(g)+3 O2(g)=2CO2 (g)+4H2O(g) Δ H2=-1352kJ/mol
写出CO2和H2生成1molCH3OH(g)的热化学方程式_____________________________。
【答案】 (1) -92 (2) ①10mol2/L2 ②逆向 (3)bc (4) ①4OH--4e-=2H2O+O2↑② 溶液中HCO3-存在电离平衡:③HCO3-![]() H++CO32-(1分),阴极H+放电,c(H+)减小平衡右移CO32-再生(1分)答案2:阴极H+放电使c(H+)增大(1分),OH-与HCO3-反应生成CO32-(1分) ③ CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-50kJ/mol
H++CO32-(1分),阴极H+放电,c(H+)减小平衡右移CO32-再生(1分)答案2:阴极H+放电使c(H+)增大(1分),OH-与HCO3-反应生成CO32-(1分) ③ CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-50kJ/mol
【解析】(1)本题考查焓变与键能的关系,△H=反应物键能总和-生成物键能总和=(946+3×436-2×3×391)kJ·mol-1=-92kJ·mol-1;(2)本题考查化学平衡常数的计算,
① N2(g)+3H2(g) ![]() 2NH3(g)
2NH3(g)
起始(mol·L-1)0.6 0.5 0
变化: 0.6×1/6 0.3 0.2
平衡: 0.5 0.2 0.2
根据化学平衡常数的定义,K=c2(NH3)/[c3(H2)×c(N2)]=0.22/(0.23×0.5)=10,②恒温恒压下,再通入0.9molN2,体积增大,浓度减小,平衡向逆反应方向进行;(3)本题考查化学平衡图像,a、根据勒夏特列原理,正反应方向是放热反应,等压下,升高温度,平衡向逆反应反应进行,N2的体积分数增大,即T2>T1,化学平衡常数只受温度影响,温度不变,化学平衡常数不变,即KA<KB=KC, 故错误;b、增大压强,平衡向正反应方向进行,因此C点氢气的浓度小于B点氢气浓度,故正确;c、根据密度的定义,组分都是气体,气体质量不变,A→B,气体物质的量减小,体积减小,即B点的密度大于A点,故正确;d、根据摩尔质量的定义,组分都是气体,气体的质量不变, A到C气体物质的量减小,即C点气体的物质的量小于A点,因此C点气体平均相对分子质量大于A点,故错误;(4)本题考查电解原理,①连有电源正极的电极为阳极,根据装置图,阳极反应式为4OH--4e-=O2↑+2H2O;②HCO3-溶液中存在HCO3-![]() H++CO32-,阴极反应式为2H++2e-=H2↑,消耗H+,促使平衡向正反应方向进行;③根据盖斯定律,①×3/2-②/2得到:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=(-484×3/2+1352/2)kJ·mol-1=-50kJ/mol 。
H++CO32-,阴极反应式为2H++2e-=H2↑,消耗H+,促使平衡向正反应方向进行;③根据盖斯定律,①×3/2-②/2得到:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=(-484×3/2+1352/2)kJ·mol-1=-50kJ/mol 。

【题目】下列分离或提纯有机物的方法正确的是( )
选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
A | 乙烷 | 乙烯 | 酸性 KMnO4溶液, 洗气 |
B | 溴苯 | 溴 | NaOH 溶液,分液 |
C | 乙酸 | 乙醇 | 金属钠,蒸馏 |
D | 乙醇 | 水 | 生石灰,过滤 |
A. A B. B C. C D. D