题目内容
下列有关晶体的叙述中错误的是( )
分析:A.石墨是层状结构,每层石墨中由共价键形成的最小的碳环上有六个碳原子;
B.氯化钠晶体中钠离子的配位数是6;
C.氯化铯晶体中,铯离子的配位数是8,每个Cs+周围等距离紧邻的有6个Cs+;
D.面心立方晶体中,晶胞立方体每个顶点上都有一个原子,面心上都有一个原子.
B.氯化钠晶体中钠离子的配位数是6;
C.氯化铯晶体中,铯离子的配位数是8,每个Cs+周围等距离紧邻的有6个Cs+;
D.面心立方晶体中,晶胞立方体每个顶点上都有一个原子,面心上都有一个原子.
解答:解:A.石墨是层状结构,每层石墨中,每个碳原子被3个环共用,由共价键形成的最小的碳环上有六个碳原子,所以平均每个环含有2个碳原子,故A正确;
B.氯化钠晶体中钠离子的配位数是6,所以每个Na+周围紧邻的有6个Cl-,故B正确;
C.氯化铯晶体中,铯离子的配位数是8,所以每个Cs+周围紧邻的有8个Cl-,每个Cs+周围等距离紧邻的有6个Cs+,故C正确;
D.面心立方晶体中,晶胞立方体每个顶点上都有一个原子,面心上都有一个原子,所以每个金属原子周围紧邻的金属原子有3×8×
=12,故D错误;
故选D.
B.氯化钠晶体中钠离子的配位数是6,所以每个Na+周围紧邻的有6个Cl-,故B正确;
C.氯化铯晶体中,铯离子的配位数是8,所以每个Cs+周围紧邻的有8个Cl-,每个Cs+周围等距离紧邻的有6个Cs+,故C正确;
D.面心立方晶体中,晶胞立方体每个顶点上都有一个原子,面心上都有一个原子,所以每个金属原子周围紧邻的金属原子有3×8×
| 1 |
| 2 |
故选D.
点评:本题考查了晶体结构,了解典型晶体的构型是解本题关键,离子晶体中离子配位数的判断是常考查点,也是学习难点.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
下列有关晶体的叙述中,错误的是( )
| A、在SiO2晶体中,每个Si原子与4个O原子形成共价键 | B、在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子 | C、NaCl晶体中与每个Na+距离相等且最近的Cl-有6个 | D、CsCl晶体中与每个Cs+距离相等且最近的Cl-有8个 |
(1)下列有关晶体的叙述中错误的是
A.石英晶体中的硅原子以sp2杂化方式与周围的氧原子形成共价键
B.氯化钠晶体中每个Na+或Cl-周围紧邻的有6个Cl-或Na+
C.在CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cl-等距离紧邻的也有8个Cs+
D.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子
(2)已知MgO的晶体结构属于NaCl型.某同学画出的MgO晶胞结构示意图如图1所示,请改正图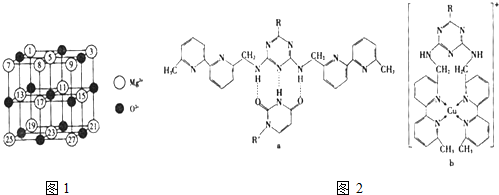
中错误: .(用文字表述)
(3)第三周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因: .
(4)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合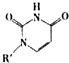 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:
分析a和b中微粒间的相互作用(包括化学键和分子间相互作用)的差异,试指出
其不同点:a中含 ,b中含 .(用“氢键”、“配位键”、“极性键”、“非极性键”等填空)
A.石英晶体中的硅原子以sp2杂化方式与周围的氧原子形成共价键
B.氯化钠晶体中每个Na+或Cl-周围紧邻的有6个Cl-或Na+
C.在CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cl-等距离紧邻的也有8个Cs+
D.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子
(2)已知MgO的晶体结构属于NaCl型.某同学画出的MgO晶胞结构示意图如图1所示,请改正图

中错误:
(3)第三周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
(4)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合
 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:分析a和b中微粒间的相互作用(包括化学键和分子间相互作用)的差异,试指出
其不同点:a中含