题目内容
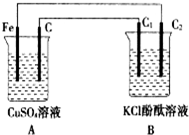 按如图装置进行实验,并回答下列问题(C、C1、C2均为石墨电极).
按如图装置进行实验,并回答下列问题(C、C1、C2均为石墨电极).(1)判断装置的名称:A池为
(2)铁极为
(3)当C2极产生2.24L气体(标准状态)时,CuSO4溶液的质量
分析:(1)A装置能自发的进行氧化还原反应,且符合原电池构成条件,为原电池,B为电解池;
(2)A中,铁易失电子发生氧化反应而作负极,碳作正极,石墨棒C2为阴极,阴极上氢离子得电子发生还原反应;
(3)放电时,A电池中负极上铁失电子生成亚铁离子,正极上铜离子得电子生成铜,结合串联电路中转移电子相等计算.
(2)A中,铁易失电子发生氧化反应而作负极,碳作正极,石墨棒C2为阴极,阴极上氢离子得电子发生还原反应;
(3)放电时,A电池中负极上铁失电子生成亚铁离子,正极上铜离子得电子生成铜,结合串联电路中转移电子相等计算.
解答:解:(1)A装置能自发的进行氧化还原反应,且符合原电池构成条件,为原电池,B电池有外接电源,为电解池,故答案为:原电池;
(2)A中,铁易失电子发生氧化反应而作负极,电极反应式为Fe-2e-=Fe2+;石墨棒C2和原电池的负极相连为阴极,氢离子放电生成氢气,导致溶液中氢氧根离子浓度增大,碱性增强,使酚酞变红,所以看到的现象是:有无色气体生成,无色溶液变红色,
故答案为:Fe-2e-=Fe2+;有无色气体生成,无色溶液变红色;
(3)C2极发生的电极反应为:2H++2e-→H2↑,析出2.24L(即0.1mol)气体(标准状态)时,转移电子数是0.2mol,所以铁极转移电子也为0.2mol,根据Fe-2e-=Fe2+,Fe极转移电子为0.2mol时,会有0.1mol金属Fe减少,即Fe的质量减少5.6g,正极上析出0.1molCu,其质量为6.4g,则溶液的质量减少0.8g,
故答案为:减少;0.8.
(2)A中,铁易失电子发生氧化反应而作负极,电极反应式为Fe-2e-=Fe2+;石墨棒C2和原电池的负极相连为阴极,氢离子放电生成氢气,导致溶液中氢氧根离子浓度增大,碱性增强,使酚酞变红,所以看到的现象是:有无色气体生成,无色溶液变红色,
故答案为:Fe-2e-=Fe2+;有无色气体生成,无色溶液变红色;
(3)C2极发生的电极反应为:2H++2e-→H2↑,析出2.24L(即0.1mol)气体(标准状态)时,转移电子数是0.2mol,所以铁极转移电子也为0.2mol,根据Fe-2e-=Fe2+,Fe极转移电子为0.2mol时,会有0.1mol金属Fe减少,即Fe的质量减少5.6g,正极上析出0.1molCu,其质量为6.4g,则溶液的质量减少0.8g,
故答案为:减少;0.8.
点评:本题考查了原电池和电解池,正确判断原电池及正负极是解本题关键,再根据各个电极上发生的电极反应来分析解答,知道串联电路中转移电子相等,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2010?娄底模拟)(1)以下说法正确的是
(2010?娄底模拟)(1)以下说法正确的是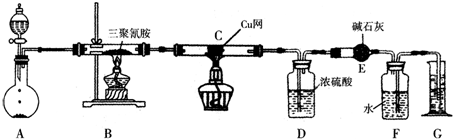
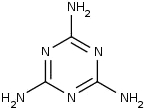

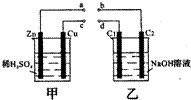 按如图装置进行实验(乙装置中的两个电极均为石墨棒),下列说法不平确的是( )
按如图装置进行实验(乙装置中的两个电极均为石墨棒),下列说法不平确的是( )