题目内容
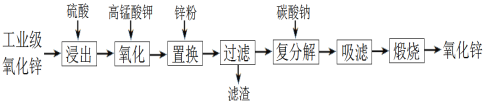
【题目】由硫铁矿“烧渣”(主要成分:Fe3O4、Fe2O3和FeO)制备绿矾(FeSO4·7H2O))的流程如图:

已知:FeS2(S的化合价为-1)难溶于水。
(1)①中加入的酸为___,滤渣2的主要成分是___。
(2)①中生成Fe3+的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O、___。
(3)检验②中Fe3+已经完全转化成Fe2+的实验方法:取适量溶液2,___。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、___。
【答案】硫酸(H2SO4) FeS2 Fe2O3+6H+=2Fe3++3H2O 向其中滴加KSCN溶液,溶液不变红 过滤、洗涤、干燥
【解析】
烧渣(主要成分:Fe3O4、Fe2O3和FeO)均溶于硫酸,溶液1含Fe2+、Fe3+,步骤②发生FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,步骤③为蒸发浓缩、冷却结晶析出绿矾,以此解答该题。
(1)因绿矾的酸根离子为硫酸根离子,则步骤①,应用硫酸来溶解烧渣;步骤②发生FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,因为FeS2难溶于水,所以滤渣2的主要成分是FeS2,故答案为:硫酸(H2SO4);FeS2;
(2)①中生成Fe3+的物质有Fe3O4、Fe2O3,则另一个离子反应为Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O;
(3)可向其中加入KSCN溶液,溶液不变红,则可说明②中Fe3+已经完全转化为Fe2+,故答案为:向其中滴加KSCN溶液,溶液不变红;
(4)通过③得到绿矾晶体的实验操作:加热浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:过滤、洗涤、干燥。

【题目】一定温度下,向容积为2 L的密闭容器中充入一定量的气体A和气体B,发生反应: 2A(g)+B(g) ![]() 2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是
2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是
反应时间/min | n(A)/mol | n(B)/mol |
0 | 0.10 | 0.060 |
t1 | 0.012 | |
t2 | 0.016 |
A. 在0~t1 min内的平均反应速率为v(C)=0.088/t1 molL-1min-1
B. 其他条件不变,起始时向容器中充入0.10 mol C和0.010 mol B,平衡时n(A)=0.012 mol
C. 保持其他条件不变,升高温度,平衡时c(A)=0.0070 molL-1,则反应的ΔH>0
D. 相同温度下,起始时向容器中充入0.15mol A和0.090mol B,平衡时A转化率大于88%