题目内容
下列实验中正确的是
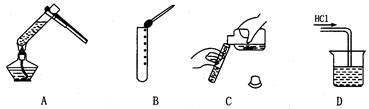
| A.用碳化钙和饱和食盐水反应制取乙炔 |
| B.将等物质的量的乙醇和乙酸放在烧瓶里加热蒸馏,制乙酸乙酯 |
| C.将醋酸钠晶体与干燥的碱石灰按一定的质量比混合后放在试管中加热制甲烷 |
| D.将苯和少量溴水放在烧瓶里并加入少量铁屑微热制溴苯 |
A
A.一般不用水与碳化钙反应制乙炔,因反应剧烈,不易控制,而用饱和食盐水可得到平缓的乙炔气流;B.酯化反应必须有浓H2SO4存在;C.应使用无水CH3COONa与碱石灰反应,有水不利CH4的生成,甚至得不到CH4;D.必须用苯与液溴在铁做催化剂条件下才能产生溴苯。

练习册系列答案
相关题目
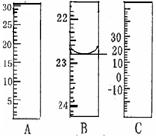
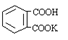 用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。
用基准物质来标定,邻苯二甲酸氢钾( ,,相对分子质量为204.0)是常用的基准物质。某学生用邻苯二甲酸氢钾测定未知NaOH溶液的浓度。在本实验中达到滴定终点时,溶液的pH约为9.1。