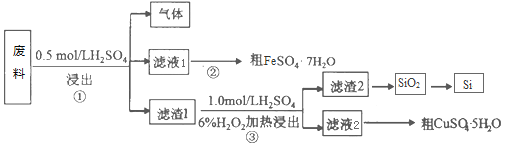
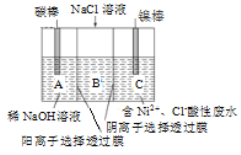
题目内容
【题目】某同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略)。请按要求回答下列问题:
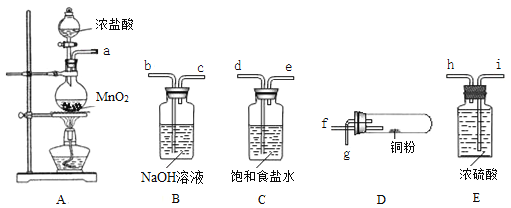
(1)装置A烧瓶中发生反应的化学方程式为_____________________________________。
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→______________________。
(3)装置B中发生反应的离子方程式为________________________,装置C中饱和食盐水的作用是__________________________________。
(4)加热装置D时,铜粉发生反应的化学方程式为____________________________。
(5)比较下列两组实验,你认为下列说法正确的是_____(填序号)。
实验①:将足量的二氧化锰与含0.4molHCl的浓盐酸反应。
实验②:将8.7g二氧化锰与足量的浓盐酸反应。
A.①产生的氯气多 B.产生的氯气一样多
C.②产生的氯气多 D.无法判断
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O d e i h f g b Cl2+2OH﹣═Cl﹣+ClO﹣+H2O 除去氯化氢,减小氯气的溶解性 Cl2+Cu
MnCl2+Cl2↑+2H2O d e i h f g b Cl2+2OH﹣═Cl﹣+ClO﹣+H2O 除去氯化氢,减小氯气的溶解性 Cl2+Cu![]() CuCl2 C
CuCl2 C
【解析】
氯气和铜粉反应的实验:MnO2与浓盐酸制取的Cl2含有HCl和H2O,用饱和食盐水除去HCl,用浓硫酸除去H2O,然后Cl2与Cu反应,最后用NaOH溶液吸收未反应的Cl2,防止污染空气;二氧化锰与浓盐酸反应生成氯气,随反应进行浓盐酸变为稀盐酸,二氧化锰不与稀盐酸反应,对于实验①,将足量的二氧化锰与含HCl0.4mol浓盐酸反应产生的氯气,HCl不能完全反应,假定HCl完全反应,计算生成的氯气的物质的量,实际氯气小于该值,对于实验②,将0.1mol二氧化锰与足量的浓盐酸反应产生的氯气,二氧化锰完全反应,根据二氧化锰结合方程式计算生成的氯气的物质的量。
(1)装置A中制取氯气,二氧化锰与浓盐酸发生反应生成氯化锰、氯气、水,反应方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)按照气体流向由左到右,仪器连接顺序为Cl2发生装置→除去HCl气体装置→干燥装置→制备装置→多余Cl2处理装置,MnO2与浓盐酸制取的Cl2含有HCl和H2O,用饱和食盐水除去HCl,用浓硫酸除去H2O,然后Cl2与Cu反应,最后用NaOH溶液吸收未反应的Cl2,防止污染空气,所以按气流方向各仪器接口顺序是:a→d→e→i→h→f→g→b,故答案为:d→e→i→h→f→g→b;
(3)装置B中为氢氧化钠吸收氯气生成氯化钠和次氯酸钠的反应,离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故答案为:Cl2+2OH-═Cl-+ClO-+H2O;
装置C中饱和食盐水的作用是除去氯化氢,减小氯气的溶解性,故答案为:除去氯化氢,减小氯气的溶解性;
(4)加热时Cu与Cl2发生化合反应生成CuCl2,反应的化学方程式为Cu+Cl2![]() CuCl2;故答案为:Cu+Cl2
CuCl2;故答案为:Cu+Cl2![]() CuCl2
CuCl2
(5)对于实验①,将足量的二氧化锰与含HCl0.4mol浓盐酸反应产生的氯气,HCl不能完全反应,假定HCl完全反应,根据反应方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O可知,含HCl0.4mol浓盐酸完全反应生成氯气为0.4mol×1/4=0.1mol,实际氯气小于0.1mol;对于实验②,将0.1mol二氧化锰与足量的浓盐酸反应产生的氯气,二氧化锰完全反应,根据反应方程式可知,生成氯气为0.1mol,实验②生成的氯气大于实验①生成的氯气,故选C,故答案为:C。
MnCl2+Cl2↑+2H2O可知,含HCl0.4mol浓盐酸完全反应生成氯气为0.4mol×1/4=0.1mol,实际氯气小于0.1mol;对于实验②,将0.1mol二氧化锰与足量的浓盐酸反应产生的氯气,二氧化锰完全反应,根据反应方程式可知,生成氯气为0.1mol,实验②生成的氯气大于实验①生成的氯气,故选C,故答案为:C。

 阅读快车系列答案
阅读快车系列答案【题目】某小组用下图所示装置对Cl2与Na2S2O3溶液的反应进行探究(气密性已检验)。
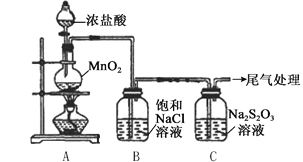
实验操作和现象:
操作 | 现象 |
打开分液漏斗活塞,滴加一定量浓盐酸,加热 | i. A中有黄绿色气体生成,C中液面上方有白雾,溶液中开始出现少量浑浊; ii. 一段时间后,C中产生大量黄色沉淀。 |
用湿润的淀粉碘化钾试纸检验C中白雾 | 淀粉碘化钾试纸变蓝 |
C中浊液过滤后,取少量滤液用盐酸酸化,滴加氯化钡溶液 | 有白色沉淀生成 |
查阅资料:a. S2O32-有较强的还原性
b. 酸性条件下S2O32-迅速分解为S和SO2
(1)A中发生反应的离子方程式是__________。
(2)B中饱和NaCl溶液的作用是_______。
(3)C中生成黄色沉淀的离子方程式是__________。
(4)为检验C中是否有SO2生成,需进行的操作是_______。
(5)C中滤液与氯化钡溶液反应生成白色沉淀,甲同学认为利用该现象可证明Na2S2O3被Cl2氧化,反应的离子方程式是__________。
(6)乙同学认为,C中滤液用硝酸酸化后滴加硝酸银溶液,若有白色沉淀,也能证明Na2S2O3被Cl2氧化,丙同学认为不能证明,理由是__________。