题目内容
用如图所示实验装置完成相应的实验,不能达到实验目的是 
- A.装置①可用于实验室制氨气后的尾气吸收
- B.装置②可用于除去Cl2中的HCl
- C.装置③可用于在铁制品表面镀锌
- D.装置④可用于除去NO中的NO2
B
分析:①四氯化碳密度比稀硫酸大,氨气不溶于四氯化碳;②氯气和HCl都与NaOH溶液反应;③该装置为电镀装置,在铁制品表面镀锌,锌作阳极;④NO2与水反应可生成NO.
解答:A.氨气不溶于四氯化碳,不会发生倒吸,氨气与稀硫酸发生反应,达到氨气被充分吸收的目的,故A不选;
B.氯气和HCl都与NaOH溶液反应,不能达到实验目的,故B选;
C.在铁制品表面镀锌时锌作阳极,用含有锌离子的电解质溶液作电解质,铁制品作阴极,能达到实验目的,故C不选;
D.NO2与水反应可生成NO,可达到实验目的,故D不选.
故选B.
点评:本题考查化学实验方案的评价,题目难度不大,注意把握相关物质的性质的异同、电解原理及应用,把握气体除杂的原则.
分析:①四氯化碳密度比稀硫酸大,氨气不溶于四氯化碳;②氯气和HCl都与NaOH溶液反应;③该装置为电镀装置,在铁制品表面镀锌,锌作阳极;④NO2与水反应可生成NO.
解答:A.氨气不溶于四氯化碳,不会发生倒吸,氨气与稀硫酸发生反应,达到氨气被充分吸收的目的,故A不选;
B.氯气和HCl都与NaOH溶液反应,不能达到实验目的,故B选;
C.在铁制品表面镀锌时锌作阳极,用含有锌离子的电解质溶液作电解质,铁制品作阴极,能达到实验目的,故C不选;
D.NO2与水反应可生成NO,可达到实验目的,故D不选.
故选B.
点评:本题考查化学实验方案的评价,题目难度不大,注意把握相关物质的性质的异同、电解原理及应用,把握气体除杂的原则.

练习册系列答案
相关题目

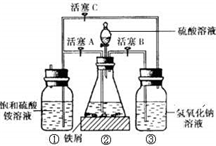 摩尔盐[(NH4)2SO4?FeSO4?6H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用如图所示的实验装置来制取摩尔盐,实验步骤如下,回答下列问题:
摩尔盐[(NH4)2SO4?FeSO4?6H2O]在空气中比一般亚铁盐稳定,是化学分析中常用的还原剂.某研究性学习小组用如图所示的实验装置来制取摩尔盐,实验步骤如下,回答下列问题: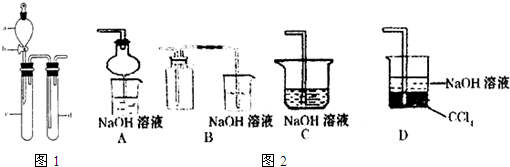
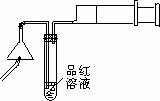
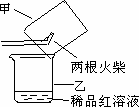
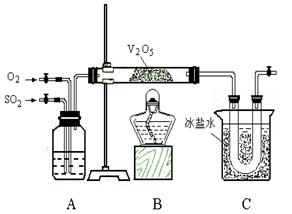
 束时得到b g 三氧化硫,该实验中二氧化硫的转化率不小于_________________;
束时得到b g 三氧化硫,该实验中二氧化硫的转化率不小于_________________; 。
。