题目内容
(8分)由H2、C2H4、C2H2组成的1L混合气体在一定条件下发生加成反应后,气体总体积变成XL。请回答(气体体积均在标准状况下测定):
(1)当反应后三种气体均无剩余时,X的取值范围是 ________________:若X=0.4时,原混合气体中H2、C2H4、C2H2的体积比为________________。
(2)当X=0.6时,且反应后混合气体密度为0.714g/L时,原混合气体H2、C2H4、C2H2的体积比为 ________________________。
(1)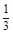 <x<
<x<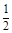 (2)3∶1∶1 (3)7∶2∶1
(2)3∶1∶1 (3)7∶2∶1
解析(1)乙烯、乙炔都和氢气发生加成反应,有关的方程式为H2+CH2=CH2 CH3CH3、2H2+C2H2
CH3CH3、2H2+C2H2 CH3CH3。因此如果全部是由氢气和乙烯构成的,则X=0.5L;如果全部是由氢气和乙炔构成的,则X=1/3L,因此X的范围是
CH3CH3。因此如果全部是由氢气和乙烯构成的,则X=0.5L;如果全部是由氢气和乙炔构成的,则X=1/3L,因此X的范围是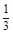 <x<
<x<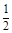 ;设原混合气中H2、C2H4、C2H2的体积分别是abc,则有b+2c=a、b+c=0.4、a+b+c=1,解得a=0.6,b=c=0.2,所以原混合气体中H2、C2H4、C2H2的体积比为3∶1∶1。
;设原混合气中H2、C2H4、C2H2的体积分别是abc,则有b+2c=a、b+c=0.4、a+b+c=1,解得a=0.6,b=c=0.2,所以原混合气体中H2、C2H4、C2H2的体积比为3∶1∶1。
(2)反应后气体的平均摩尔质量是0.714g/L×22.4L/mol=16,所以氢气一定是过量的。及反应后的气体是氢气和乙烷的混合气,二者的体积之比是1︰1,所以氢气是0.3L,乙烷是0.3L。设原混合气中H2、C2H4、C2H2的体积分别是abc,则有b+2c=1-b-c-0.3、b+c=0.3、a+b+c=1,解得a=0.7,b=0.2,c=0.1,所以原混合气体中H2、C2H4、C2H2的体积比为7∶2∶1。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目

 2NH3的△H
2NH3的△H
 2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下, 测得反应达
2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下, 测得反应达 +
+ =1
=1


 2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下, 测得反应达
2HI(g) △H=-14.9 kJ·mol-1),在恒温、恒容条件下, 测得反应达 +
+ =1
B.2
=1
B.2 C.a+b=14.9
D.c1=c2=c3
C.a+b=14.9
D.c1=c2=c3