题目内容
16.下列判断正确的是( )| A. | 向某溶液中加入AgNO3溶液,生成白色沉淀,可确定有Cl-存在 | |
| B. | 向某溶液中加入氢氧化钠溶液,产生蓝色沉淀,可确定有Cu2+存在 | |
| C. | 向某溶液中加入BaCl2溶液,生成白色沉淀,加稀盐酸沉淀不溶解,可确定有SO${\;}_{4}^{2-}$存在 | |
| D. | 向某溶液中加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO${\;}_{3}^{2-}$ |
分析 A.可能生成碳酸银、硫酸银等沉淀;
B.氢氧化铜为蓝色沉淀;
C.可能生成AgCl沉淀;
D.可能含有HCO3-.
解答 解:A.加入AgNO3溶液,生成白色沉淀,不一定生成AgCl沉淀,可能生成碳酸银、硫酸银等沉淀,应加入硝酸酸化,故A错误;
B.氢氧化铜为蓝色沉淀,可确定有Cu2+存在,故B正确;
C.检验硫酸根离子,应先加入盐酸,如无现象,再加入氯化钡,如生成沉淀,可说明含有硫酸根离子,故C错误;
D.HCO3-也可与酸反应生成二氧化碳气体,故D错误;
故选B.
点评 本题考查化学实验方案的评价,侧重离子检验的考查,涉及常见阴、阳离子的检验,注意把握物质的性质以及检验中排除干扰因素,题目难度不大.

练习册系列答案
相关题目
6.胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得101kPa时,氢气的燃烧热是285.8kJ•mol-1,表示该反应的热化学方程式正确的是( )
| A. | H2+$\frac{1}{2}$O2═H2O△H=-285.8 kJ•mol-1 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6 kJ•mol-1 |
7.下列说法中正确的是( )
| A. | 标准状况下,22.4 L水中所含的分子数约为6.02×1023个 | |
| B. | 1 mol Cl2中含有的原子数为NA | |
| C. | 标准状况下,a L氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$×6.02×1023个 | |
| D. | 从1 L0.5 mol•L-1NaCl溶液中取出100 mL,剩余溶液中NaCl物质的量浓度为0.45 mol•L-1 |
4.被誉为“光纤之父”的华人科学家高锟获2009年诺贝尔物理学奖.关于光导纤维的说法,错误的是( )
| A. | 光导纤维的主要成分是氧化物 | |
| B. | 由石英玻璃拉制成细丝的过程是化学变化 | |
| C. | 光导纤维是利用激光传输信息的 | |
| D. | 光纤通信不容易受外界干扰,能够传播得更远 |
1.下列实验目的能达到的是( )
| A. | 将58.5gNaCl溶于1L水中可得1mol/L的NaCl溶液 | |
| B. | 将标准状况下22.4LHCl溶于1L水中可得1mol/L盐酸 | |
| C. | 将 25.0g胆矾溶于水后配成100mL溶液所得溶液浓度为1mol/L | |
| D. | 将 78gNa2O2溶于水,配成1L溶液可得到浓度为1mol/L溶液 |
8.下列有关化学用语的表示正确的是( )
| A. | 中子数为18的氯原子:${\;}_{17}^{35}$Cl | B. | 二氧化碳分子的比例模型: | ||
| C. | HClO的电子式: | D. | 对羟基苯甲醛的结构简式:OH- -CHO -CHO |
5.下列溶液中溶质物质的量浓度为1mol•L-1的是( )
| A. | 将40g NaOH溶解在1L水中 | |
| B. | 将22.4L HCl气体溶于水配成1L溶液 | |
| C. | 将0.1L 10 mol•L-1浓硫酸加入0.9L水中 | |
| D. | 将25g 胆矾溶于水配成100mLCuSO4溶液 |
6.下列物质属于酚类的是( )
| A. |  | B. | 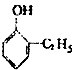 | C. |  | D. | 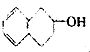 |