题目内容
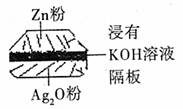
如图为一种钮扣微型电池,其电极分别为Ag2O和Zn电解质溶液是KOH溶液,俗称银锌电池,该电池的电极反应式为:Zn+Ag2O═ZnO+2Ag根据以上提供的资料,下列说法正确的是( )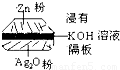
A.溶液中OH-向正极移动
B.放电时正极附近溶液的PH值升高
C.电池负极的电极反应为:Zn-2e-═Zn2+
D.电池工作时,生成1mol Ag就有2mol电子转移
【答案】分析:根据总方程式可知Zn为原电池的负极,发生反应为Zn+2OH--2e-═ZnO+H2O,Ag2O为原电池的正极,发生反应为Ag2O+H2O+2e-═2Ag+2OH-,原电池中电流从正极流向负极,溶液中阴离子流向负极,阳离子流向正极.
解答:解:A.溶液中OH-向负极移动,故A错误;
B.正极反应为Ag2O+H2O+2e-═2Ag+2OH-,放电时正极附近溶液的PH值升高,故B正确;
C.负极电极反应为Zn+2OH-=ZnO+H2O+2e-,故C错误;
D.正极电极反应为:Ag2O+H2O+2e-=2Ag+2OH-,当电路中每通过1mol电子,则生成1molAg,故D错误.
故选B.
点评:本题考查原电池知识,题目难度不大,注意根据电极反应判断原电池的正负极以及电池反应.
解答:解:A.溶液中OH-向负极移动,故A错误;
B.正极反应为Ag2O+H2O+2e-═2Ag+2OH-,放电时正极附近溶液的PH值升高,故B正确;
C.负极电极反应为Zn+2OH-=ZnO+H2O+2e-,故C错误;
D.正极电极反应为:Ag2O+H2O+2e-=2Ag+2OH-,当电路中每通过1mol电子,则生成1molAg,故D错误.
故选B.
点评:本题考查原电池知识,题目难度不大,注意根据电极反应判断原电池的正负极以及电池反应.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
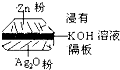 如图为一种钮扣微型电池,其电极分别为Ag2O和Zn电解质溶液是KOH溶液,俗称银锌电池,该电池的电极反应式为:Zn+Ag2O═ZnO+2Ag根据以上提供的资料,下列说法正确的是( )
如图为一种钮扣微型电池,其电极分别为Ag2O和Zn电解质溶液是KOH溶液,俗称银锌电池,该电池的电极反应式为:Zn+Ag2O═ZnO+2Ag根据以上提供的资料,下列说法正确的是( )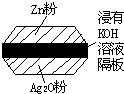 如图为一种钮扣微型电池,其电极分别为Ag2O和Zn,电解质溶液是KOH溶液,俗称银锌
如图为一种钮扣微型电池,其电极分别为Ag2O和Zn,电解质溶液是KOH溶液,俗称银锌