题目内容
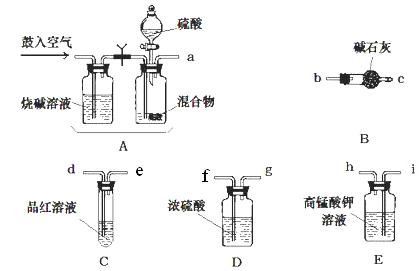
有NH4HCO3、NH4Cl、Na2CO3·xH2O混合物11.62g,加入44 mL5mol/L过量NaOH溶液共热,放出气体通过碱石灰后测得为3.36L(标准状况),向上述溶液中加入30 mL 2.5mol/L H2SO4,并加热使气体全部排出,测得体积为1.344L(标准状况),最后把所得溶液稀释到100 mL,测得pH=1,求原混合物中各物质的量和x的数值。
x=7
解析:
本题涉及的化学反应较多,我们可用图示表示如下:

若按常规方法来解,则比较繁琐,但如若我们抓住反应前后N元素、C元素以及溶液中离子电荷的守恒关系,由守恒关系列方程,解题则往往较简捷。
设混合物中NH4HCO3、NH4Cl、Na2CO3·xH2O的物质的量各为a、b、c。
则由总质量可得
79g/mol·a+53.5g/mol·b+(106g/mol+18g/mol·x)c=11.62g ①

因最终得到的是Na2SO4、H2SO4、NaCl的混合液,故由溶液中离子电荷守恒得:
![]()
2c+5mol/L×0.044L+0.1mol/L×0.1L
=2×2.5mol/L×0.03L+b ④
解 联立方程式①②③④得:

练习册系列答案
相关题目
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中.然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固.由此可见( )
| A、NH4HCO3和盐酸的反应是放热反应 | B、该反应中,热能转化为产物内部的能量 | C、反应物的总能量高于生成物的总能量 | D、反应的热化学方程式为:NH4HCO3+HCl→NH4Cl+CO2↑+H2O-Q |
将盛有NH4HCO3粉末的小烧杯放入盛有少量醋酸的大烧杯中.然后向小烧杯中加入盐酸,反应剧烈,醋酸逐渐凝固.由此可见( )
| A、复分解反应都是吸热反应 | B、NH4HCO3和盐酸的反应是吸热反应 | C、反应物的总能量高于生成物的总能量 | D、反应的热化学方程式为:NH4HCO3+HCl═NH4Cl+CO2↑+H2O△H>0 |
 。回答以下问题:
。回答以下问题:
 。回答以下问题:
。回答以下问题: