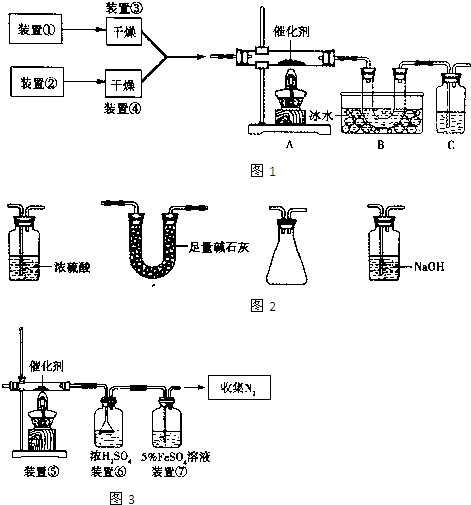
题目内容
下列离子方程式表达正确的是
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B.小苏打溶液呈碱性的原因:HCO3-+H2O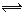 H3O++CO32-
H3O++CO32-
C.溴化亚铁溶液中通入足量氯气:2Fe2++ 4Br-+ 3Cl2 = 2Fe3++2 Br2 + 6Cl-
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O
【答案】
C
【解析】
试题分析:A、漏写Fe3+与I-的反应,错误;B、小苏打溶液呈碱性的原因是碳酸氢钠水解造成的,应为:HCO3-+H2O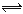 OH-+H2CO3,错误;D、Al3+与少量Ba(OH)2溶液溶液反应应生成氢氧化铝沉淀,错误;选C
OH-+H2CO3,错误;D、Al3+与少量Ba(OH)2溶液溶液反应应生成氢氧化铝沉淀,错误;选C
考点:考查离子方程式正误判断

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目