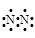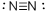题目内容
金属钾的冶炼可采用如下方法:2KF+CaC2 CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )
 CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )| A.该反应的氧化剂是KF,氧化产物是K |
| B.该反应能说明C的还原性大于K |
| C.电解KF溶液不可能制备金属钾 |
| D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1 |
C
试题分析:分析氧化还原反应注意①标清变价元素的化合价②熟记氧化还原反应的基本概念和基本规律③突破电子转移;该反应中钾元素的化合价由+1价降为0价,被还原,KF为氧化剂,K为还原产物;碳元素的化合价由—1价升高到0价,被氧化,CaC2作还原剂,C是氧化产物;A、该反应的氧化剂是KF,氧化产物是C,错误;B、该反应的还原剂为CaC2,还原产物为K,不能说明C的还原性大于K,错误;C、电解KF溶液,阳离子H+放电,阴离子OH—放电,不可能制备金属钾,正确;D、CaC2、CaF2均为离子化合物,CaF2中阴、阳离子个数比为2∶1,而CaC2中阴、阳离子个数比为1∶1,错误。

练习册系列答案
相关题目
 TiCl4+2CO;②TiCl4+2Mg
TiCl4+2CO;②TiCl4+2Mg