题目内容
为了净化和收集由盐酸和大理石制得的CO2气体,从下图中选择合适的的装置并连接。合理的是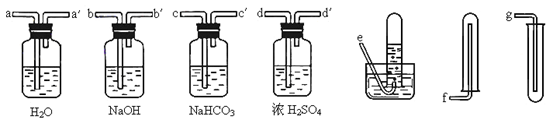
| A.a-a′→d-d′→e | B.b-b′→d-d′→g |
| C.c-c′→d-d′→g | D.d-d′→c-c′→f |
C
解析

用右图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是
| 选项 | 甲 | 乙 | 丙 | 试管中现象 | 结论 |
| A | 稀硫酸 | 亚硫酸钠 | 溴水 | 橙色褪去 | SO2具有漂白性 |
| B | 饱和食盐水 | 电石 | 酸性 KMnO4溶液 | 紫色褪去 | 乙炔可发生氧化反应 |
| C | 醋酸 | 碳酸钠 | BaCl2溶液 | 变浑浊 | 醋酸酸性强于碳酸 |
| D | 浓氨水 | 生石灰 | AgNO3溶液 | 无明显现象 | NH3与 AgNO3溶液不反应 |
通常情况下,以下气体不能用浓硫酸干燥的是
| A.SO2 | B.Cl2 | C.HCl | D.NH3 |
用如图所示的装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是
| 选项 | 气体 | a | b | c |
| A | CO2 | 稀盐酸 | 石灰石 | 浓硫酸 |
| B | SO2 | 浓硫酸 | 铁片 | 浓硫酸 |
| C | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
| D | Cl2 | 浓盐酸 | MnO2粉末 | 浓硫酸 |
下列气体中,既可用浓H2SO4干燥,又可用固体NaOH干燥的是
| A.Cl2 | B.NH3 | C.SO2 | D.O2 |
过氧化钙晶体[CaO2·8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
Ⅰ.过氧化钙晶体的制备。
工业上生产CaO2·8H2O的主要流程如下: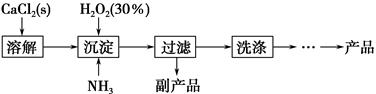
(1)用上述方法制取CaO2·8H2O的化学方程式是_________________________________。
(2)沉淀时常用冰水控制温度在10 ℃以下和通入过量的NH3,其可能原因分别是①__________________________;②_____________________________。
Ⅱ.过氧化钙晶体含量的测定。
准确称取0.300 0 g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1 H2SO4,用0.020 0 mol·L-1 KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O
滴定终点观察到的现象为_______________________________________。
(4)根据表中数据,计算产品中CaO2·8H2O的质量分数(写出计算过程)。
KMnO4标准溶液滴定数据
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.300 0 | 1.02 | 24.04 |
| 2 | 0.300 0 | 2.00 | 25.03 |
| 3 | 0.300 0 | 0.20 | 23.24 |
用如图所示装置制取表格中的四种干燥、纯净的气体(必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中正确的是 ( )。
| 选项 | 气体 | a | b | c | d |
| A | SO2 | 浓硫酸 | Cu | H2O | 浓硫酸 |
| B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
| C | NH3 | 饱和NH4Cl溶液 | 消石灰 | 空集气瓶 | 固体NaOH |
| D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |
下列气体:①NH3 ②NO2 ③NO ④O2 ⑤SO2中,适于用下图装置制取和收集的气体是( )
| A.①② | B.②③ | C.③④ | D.②⑤ |



