题目内容
【题目】工业废水中常含有一定量的Cr2O72-,易被人体吸收累积而导致肝癌。处理工业含铬废水的方法通常是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀。已知元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72(橙红色)、CrO42(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体。
(1)Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是____
(2)利用硫酸工业废气中的SO2可以处理酸性含铬废水,用离子方程式表示反应原理:_______________
(3)Cr3+在强碱中可被双氧水氧化为CrO42-,发生反应的离子方程式为_________________
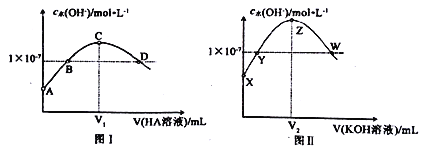
(4)CrO42和Cr2O72在溶液中可相互转化。室温下,初始浓度为1.0 mol·L1 的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。
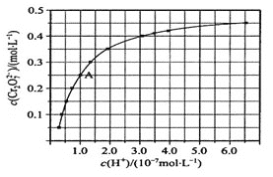
①由图可知,溶液酸性增大,CrO42的平衡转化率_________(填“增大“减小”或“不变”),
② 据A点数据,计算出该转化反应的平衡常数__________。
【答案】蓝紫色溶液变浅,同时有灰蓝色沉淀生成,然后沉淀逐渐溶解形成绿色溶液 Cr2O72- +3SO2 +2H+ =2Cr3+ +3SO42- +H2O 2Cr3++3H2O2+10OH-=2CrO42- +8H2O 增大 1.0×1014 (mol·L1)-3
【解析】
(1)溶液Cr3+(蓝紫色)和氢氧化钠溶液反应生成Cr(OH)3为难溶于水的灰蓝色固体,和氢氧化铝性质相似为两性氢氧化物,溶于强碱;
(2)利用氧化还原反应中得失电子守恒、电荷守恒和原子守恒进行配平;
(3)利用守恒原则配平离子方程式;
(4)由图可知,溶液酸性增大,平衡2CrO42-+2H+![]() Cr2O72-+H2O正向进行,CrO42的平衡转化率增大;根据平衡常数的公式计算。
Cr2O72-+H2O正向进行,CrO42的平衡转化率增大;根据平衡常数的公式计算。
(1)Cr3+与Al3+的化学性质相似可知Cr2(SO4)3溶液中逐滴加入NaOH溶液,先生成Cr(OH)3灰蓝色沉淀,继续加入NaOH后沉淀溶解,生成绿色Cr(OH)4-;
故答案为:蓝紫色溶液变浅,同时有灰蓝色沉淀生成,然后沉淀逐渐溶解形成绿色溶液。
(2)利用SO2的还原性将废液中的Cr2O72-还原成Cr3+,则Cr2O72-将SO2氧化为SO42-,根据得失电子守恒、电荷守恒和原子守恒,配平离子方程式为:Cr2O72- +3SO2+2H+=2Cr3+ +3SO42-+H2O,故答案为:Cr2O72- +3SO2+2H+=2Cr3+ +3SO42-+H2O。
(3)Cr3+在强碱中可被双氧水氧化为CrO42-,发生反应的离子方程式为2Cr3++3H2O2+10OH-=2CrO42- +8H2O,故答案为:2Cr3++3H2O2+10OH-=2CrO42- +8H2O。
(4)①由图可知,溶液酸性增大,平衡2CrO42-+2H+![]() Cr2O72-+H2O正向进行,CrO42的平衡转化率增大,故答案为:增大。
Cr2O72-+H2O正向进行,CrO42的平衡转化率增大,故答案为:增大。
②A点Cr2O72-的浓度为0.25mol/L,根据Cr元素守恒可知CrO42-的浓度为0.5mol/L;H+浓度为1×10-7mol/L;此时该转化反应的平衡常数为c(Cr2O72-)/c2(CrO42-)c2(H+)=0.25/0.52×(1×10-7)2=1.0×1014(mol·L1)-3,
故答案为:1.0×1014(mol·L1)-3。

 名校课堂系列答案
名校课堂系列答案【题目】下列实验操作对应的现象不符合事实的是
|
|
|
|
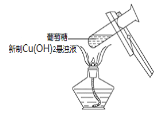
A.少量二氧化硫通入氯化钡溶液中,产生白色沉淀亚硫酸钡 | B.在新制Cu(OH)2悬浊液中加入少量的葡萄糖,加热,产生砖红色沉淀 | C.将少量钠投入到无水乙醇中,钠表面有气泡产生 | D.在盛水的烧杯中加入氯化钠固体,小灯泡会逐渐亮起来 |
A. AB. BC. C...D. D