题目内容
【题目】如下图所示是实验室制取SO2并验证SO2某些性质的装置图。试回答:
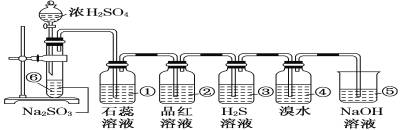
(1)⑥中发生反应的化学方程式为______。
(2)①中的实验现象为_______。
(3)②中的实验现象为______,证明SO2有_____性。
(4)③中的实验现象是______,证明SO2有______性。
(5)④中的实验现象是_____,证明SO2有______性。
(6)⑤的作用是______,反应的化学方程式为_______。
【答案】Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O 石蕊溶液变红 品红溶液褪色 漂白 有黄色沉淀产生 氧化 溴水褪色 还原 吸收多余的二氧化硫 SO2+2NaOH=Na2SO3+H2O
【解析】
根据实验装置分析可知,⑥中Na2SO3和浓H2SO4发生反应Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O制取SO2,①为检验SO2的酸性的装置,②为检验SO2的漂白性的装置,③为检验SO2的氧化性的装置,④为检验SO2的还原性的装置,⑤为尾气处理装置,据此分析解答。
(1)⑥中为亚硫酸钠和浓硫酸反应生成二氧化硫气体,反应的化学方程式为Na2SO3+H2SO4(浓)=Na2SO4+H2O+SO2↑;
(2)二氧化硫溶于水和水反应生成亚硫酸,亚硫酸为二元中强酸,可以使紫色石蕊试液变红,即①中的实验现象为石蕊试液变红;
(3)二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故二氧化硫具有漂白性;
(4)SO2中+4价S具有氧化性,硫化氢中-2价S具有还原性,二氧化硫能把硫化氢氧化成单质硫,本身被还原成单质硫,反应方程式为SO2+2H2S=3S↓+2H2O,所以③中的实验现象是有淡黄色沉淀生成,证明了SO2具有氧化性;
(5)二氧化硫具有还原性,能被溴水氧化而使其褪色;
(6)二氧化硫有毒,不能直接排放到空气中,二氧化硫能够与氢氧化钠反应生成亚硫酸钠和水,所以可以用氢氧化钠溶液吸收二氧化硫,即⑤的作用是吸收多余的二氧化硫,防止二氧化硫污染环境,反应的化学方程式为SO2+2NaOH=Na2SO3+H2O。

 智慧小复习系列答案
智慧小复习系列答案