题目内容
某温度时,BaSO4在水中的沉淀溶解平衡曲线如右图所示。下列说法正确的是( )
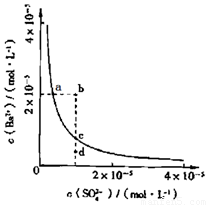
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
【答案】
C
【解析】略

练习册系列答案
相关题目
题目内容
某温度时,BaSO4在水中的沉淀溶解平衡曲线如右图所示。下列说法正确的是( )

A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
C
【解析】略
