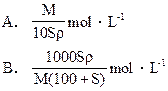题目内容
根据有关信息:2SO2(g)+O2(g) 2SO3(g)+196.7KJ;某种硝酸钙晶体可表示为Ca(NO3)2·8H2O;25℃时NaHCO3的溶解度为9.6g/100g水;空气中氧气的体积分数为21%,判断下列有关数据正确的是
| A.室温下,配制2.5mol/L的NaHCO3溶液 |
| B.爆炸最强烈的坑道气中甲烷的体积分数为10.5% |
| C.用1molSO2气体与足量氧气反应放出的热量为98.35KJ |
| D.与CaO作用直接制Ca(NO3)2·8H2O所用硝酸的质量分数为50% |
D
本题综合考查常规计算。25℃时NaHCO3的溶解度为9.6g/100g水,所以饱和NaHCO3溶液的物质的量浓度约为1mol/L,所以无法配制2.5mol/L的NaHCO3溶液,A选项错误;爆炸最强烈的情况是甲烷与氧气完全反应,设甲烷体积x,则参加反应氧气的体积为2x,则甲烷的体积分数为:x/(
 +x)×100%=9.5%,B选项错误;SO2与氧气的反应是可逆反应,所以1molSO2气体不可能完全转化,则放出的热量小于98.35KJ,C选项错误。
+x)×100%=9.5%,B选项错误;SO2与氧气的反应是可逆反应,所以1molSO2气体不可能完全转化,则放出的热量小于98.35KJ,C选项错误。
练习册系列答案
相关题目