题目内容
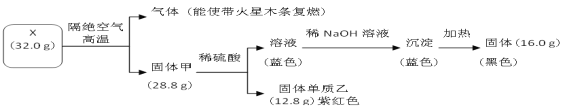
【题目】为探究黑色固体 X(仅含两种元素)的组成和性质,设计并完成如下实验:
(1)X的化学式是________________。
(2)写出固体甲与稀硫酸反应的离子方程式________________________。
【答案】CuO Cu2O+2H+=Cu+Cu2++H2O
【解析】
根据框图逆推本题:气体能使带火星的木条复燃,说明隔绝空气加热会产生氧气;固体甲遇到硫酸产生蓝色溶液和紫红色固体单质乙,说明有铜产生,进而说明X中含有铜元素和氧元素,再根据质量守恒进行解答。
(1)32.0gX隔绝空气加热分解放出的能使带火星的木条复燃的气体为氧气,质量为32.0g-28.8g=3.2g,证明X中含氧元素,28.8g固体甲和稀硫酸溶液反应生成蓝色溶液,说明含铜离子,证明固体甲中含铜元素,即X中含铜元素,铜元素和氧元素形成的黑色固体为CuO,所以X为氧化铜,本题答案: CuO;
(2)由n(CuO)=32.0g÷80gmol-1=0.4mol,结合质量守恒得到n(O2)=3.2g÷32gmol-1=0.1mol,由氧元素守恒得到甲中n(Cu): n(O)=0.4mol:(O.4mol-0.1mol×2)=2:1,固体甲的化学式为Cu2O,加稀硫酸后,产生蓝色溶液和固体单质乙,固体单质乙为Cu,蓝色溶液为硫酸铜,与稀硫酸反应的离子方程式为:Cu2O+2H+=Cu+Cu2++H2O;答案:Cu2O+2H+=Cu+Cu2++H2O。

练习册系列答案
相关题目