题目内容
(2011?广东模拟)某小组的同学对放置已久的过氧化钠的成份进行探究,请回答下列问题:
(1)反应 2Na2O2+2H2O=4NaOH+O2↑的还原剂是
(2)进行探究:
①提出假设. 假设1:全部是Na2O2 假设2:全部是Na2CO3 假设3:
②设计方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论(可不填满).限选实验试剂和仪器:蒸馏水、1moL?L-1H2SO4、澄清石灰水、淀粉-KI溶液、酚酞溶液、火柴、试管、小烧杯.
(1)反应 2Na2O2+2H2O=4NaOH+O2↑的还原剂是
Na2O2
Na2O2
(写化学式);反应2Na2O2+2CO2=2Na2CO3+O2↑中,每生成1molO2则转移了2
2
mol电子.(2)进行探究:
①提出假设. 假设1:全部是Na2O2 假设2:全部是Na2CO3 假设3:
是Na2O2与Na2CO3的混合物
是Na2O2与Na2CO3的混合物
②设计方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论(可不填满).限选实验试剂和仪器:蒸馏水、1moL?L-1H2SO4、澄清石灰水、淀粉-KI溶液、酚酞溶液、火柴、试管、小烧杯.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,滴加足量1moL?L-1 H2SO4至固体溶解,然后将内壁附有澄清石灰水的烧杯罩于试管口. | 若澄清石灰水未见浑浊,则假设1成立; 若澄清石灰水变浑浊,则 假设2或假设3成立 假设2或假设3成立 (或假设1不成立) (或假设1不成立) |
| 步骤2: | |
| 步骤3: |
分析:(1)根据Na2O2在反应中既是氧化剂又时还原剂;根据反应2Na2O2+2CO2=2Na2CO3+O2↑中2个Na2O2转移2个电子;
(2)①也可能是两者的混合物;
②根据Na2O2与硫酸反应产生氧气,Na2CO3与与硫酸反应产生二氧化碳,Na2O2具有漂白性来解答;
(2)①也可能是两者的混合物;
②根据Na2O2与硫酸反应产生氧气,Na2CO3与与硫酸反应产生二氧化碳,Na2O2具有漂白性来解答;
解答:解:因Na2O2在反应中既是氧化剂又时还原剂,因反应2Na2O2+2CO2=2Na2CO3+O2↑中2个Na2O2转移2个电子,每生成1molO2则转移了2mol电子,故答案为:Na2O2;2;
(2)①也可能是两者的混合物,故答案为:是Na2O2与Na2CO3的混合物
②因Na2O2与硫酸反应产生氧气,Na2CO3与与硫酸反应产生二氧化碳,Na2O2具有漂白性来解答,故答案为:
(2)①也可能是两者的混合物,故答案为:是Na2O2与Na2CO3的混合物
②因Na2O2与硫酸反应产生氧气,Na2CO3与与硫酸反应产生二氧化碳,Na2O2具有漂白性来解答,故答案为:
| 实验步骤 | 预期现象和结论 |
| 假设2或假设3成立,或假设1不成立 | |
| 步骤2:另取少量固体于试管中加适量蒸馏水,再滴入酚酞溶液 | 若滴入酚酞溶液后先变红后褪色则假设1或假设3成立;若红色不褪色,则假设2成立 |
点评:本题主要考查了Na2O2的性质,结合实验,考查了学生分析问题、解决问题的能力.

练习册系列答案
相关题目
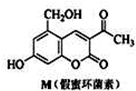 (2011?广东模拟)化合物M叫假蜜环菌甲素,它是香豆素类天然化合物.对M的性质叙述正确的是( )
(2011?广东模拟)化合物M叫假蜜环菌甲素,它是香豆素类天然化合物.对M的性质叙述正确的是( )