题目内容
【题目】硫代硫酸钠(Na2S2O3)是环保部门监测有害气体常用的一种药品,它易溶于水,遇酸易分解。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图。

实验具体操作步骤为:
①打开分液漏斗使硫酸慢慢滴下,适当调节分液漏斗的滴速,使反应产生的SO2气体较均匀的通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体。
(1)写出仪器A的名称____。
(2)写出A中发生反应的化学方程式____。
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是____。
(4)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42离子,该反应的离子方程式为____。
(5) 为了验证固体硫代硫酸钠工业产品中含有碳酸钠,选用下图装置进行实验。
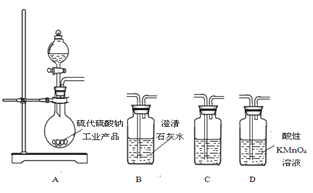
①实验装置的连接顺序依次是____(填装置的字母代号),装置C中的试剂为____。
②能证明固体中含有碳酸钠的实验现象是____。
【答案】 蒸馏烧瓶 Na2SO3 + H2SO4= Na2SO4+ SO2↑ + H2O SO2过量,溶液呈酸性,硫代硫酸钠分解,产量下降 S2O32-+4Cl2+5H2O = 2SO42-+8Cl-+10H+ ADCB 品红溶液(或高锰酸钾溶液) C中品红不褪色(或高锰酸钾溶液不褪色),B中石灰水变浑浊
【解析】试题分析:(1)根据装置图分析仪器名称;(2)硫酸与亚硫酸钠反应生成硫酸钠、二氧化硫、水;(3)SO2过量,溶液呈酸性,硫代硫酸钠遇酸易分解;(4)S2O32-被Cl2氧化成SO42,氯气被还原为Cl-;(5)硫代硫酸钠与硫酸反应生成二氧化硫;碳酸钠与硫酸反应生成二氧化碳,要验证二氧化碳生成需先用高锰酸钾溶液除去二氧化硫、用品红验证二氧化硫是否除尽、用澄清石灰水检验二氧化碳;
解析:根据以上分析,(1)仪器A的名称蒸馏烧瓶。
(2)A中硫酸与亚硫酸钠反应生成硫酸钠、二氧化硫、水的化学方程式是Na2SO3 + H2SO4= Na2SO4+ SO2↑ + H2O。
(3)SO2过量,溶液呈酸性,硫代硫酸钠遇酸易分解产量下降,所以实验中通入的SO2不能过量。
(4)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42离子,反应的离子方程式为S2O32-+4Cl2+5H2O = 2SO42-+8Cl-+10H+。
(5) 硫代硫酸钠与硫酸反应生成二氧化硫;碳酸钠与硫酸反应生成二氧化碳,要验证二氧化碳生成需先用高锰酸钾溶液除去二氧化硫、用品红验证二氧化硫是否除尽、用澄清石灰水检验二氧化碳。①实验装置的连接顺序依次是ADCB,C装置中盛放品红溶液检验二氧化硫是否除尽;②C中品红不褪色、B中石灰水变浑浊能证明固体中含有碳酸钠。