题目内容
【题目】完成以下问题:
(1)下列反应中,属于吸热反应的是______________(填数字序号)。
①煅烧石灰石制生石灰 ②燃烧木炭取暖 ③酸碱中和反应
④铝粉与氧化铁粉末在高温下反应 ⑤生石灰与水作用制熟石灰 ⑥食物因氧化而腐败
(2)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能最为E2,且E1>E2,则该反应为____(“吸热”或“放热”)反应。
②已知断开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则反应N2(g)+3H2(g)![]() 2NH3(g),若1molN2完全反应生成NH3会放出________kJ的热量。
2NH3(g),若1molN2完全反应生成NH3会放出________kJ的热量。
(3)相对分子质量为72的烷烃的分子式为______________。
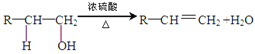
(4)有机物的结构可用“键线式”表示,如:CH3CH=CHCH3可简写为![]() 。
。![]() 可简写为
可简写为![]() 。玫瑰的香味物质中包含苧烯,苧烯的键线式如图
。玫瑰的香味物质中包含苧烯,苧烯的键线式如图![]() ,苧烯的分子式为___________。
,苧烯的分子式为___________。
【答案】 ① 放热 -92kJ C5H12 C10H16
【解析】(1)根据反应的特点和能量变化分析解答;
(2)根据反应物总能量与生成物总能量的关系判断是放热还是吸热;反应热等于断键吸收的能量和形成化学键所放出的能量的差值;
(3)根据烷烃的通式解答;
(4)将碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有1个碳原子,称为键线式。
(1)①煅烧石灰石制生石灰是吸热反应;②燃烧木炭取暖是放热反应;③酸碱中和反应是放热反应;④铝粉与氧化铁粉末在高温下发生铝热反应是放热反应;⑤生石灰与水作用制熟石灰是放热反应;⑥食物因氧化而腐败的放热反应。则属于吸热反应的是①;
(2)①若反应物的总能量为E1,生成物的总能最为E2,且E1>E2,这说明反应物的总能量高于生成物的总能量,因此该反应为放热反应。
②已知断开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则反应N2(g)+3H2(g)![]() 2NH3(g)的反应热△H=(946+3×436-2×3×391)kJ/mol=-92kJ/mol,因此1molN2完全反应生成NH3会放出92kJ的热量。
2NH3(g)的反应热△H=(946+3×436-2×3×391)kJ/mol=-92kJ/mol,因此1molN2完全反应生成NH3会放出92kJ的热量。
(3)烷烃的通式是CnH2n+2,相对分子质量为72的烷烃,则14n+2=72,解得n=5,所以分子式为C5H12。
(4)苧烯的键线式如图![]() ,则苧烯的分子式为C10H16。
,则苧烯的分子式为C10H16。