题目内容
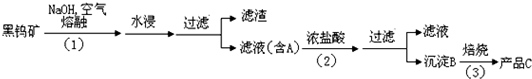
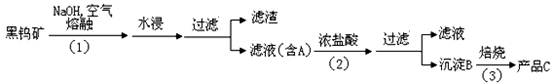
钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,有“光明使者”的美誉.钨在自然界主要以钨 (+6价) 酸盐的形式存在.有开采价值的钨矿石是白钨矿和黑钨矿.白钨矿的主要成分是钨酸钙 (CaWO4);黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成(Fe,Mn)WO4,钨酸(H2WO4)酸性很弱,难溶于水.黑钨矿传统冶炼工艺的第一阶段是碱熔法:其中 A、B、C 都是钨的化合物.回答:
(1)74W在周期表的位置是第
(2)写出上述流程中B、C 的化学式:B
(3)钨冶炼工艺的第二阶段则是用碳、氢等还原剂把氧化钨还原为金属钨.对钨的纯度要求不高时,可用碳作还原剂.写出用碳还原氧化钨制取金属钨的化学方程式:
为了获得可以拉制灯丝的高纯度金属钨,不宜用碳而必须用氢气作还原剂,为什么?
(4)仲钨酸的阱盐在热分解时会发生内在氧化还原反应,我国钨化学研究的奠基人顾冀东先生采用这一反应制得了蓝色的、非整比的钨氧化物 WO3-x. 这种蓝色氧化钨具有比表面大、易还原的优点,在制钨粉时温度容易控制,目前冶炼拉制钨丝的金属钨都用蓝色氧化钨为原料.经分析,得知蓝色氧化钨中钨的质量分数为 0.7985.
①计算 WO3-x中的x值.x=
②一般认为,蓝色氧化钨的颜色和非整比暗示了在化合物中存在五价和六价两种价态的钨.则蓝色氧化钨中这两种价态的钨原子数比为
分析:(1)根据74W的质子数可知电子数为74,核外各电子层电子数为2、8、18、32、14、2,电子层数等于周期序数;
(2)根据氢氧化铁和氢氧化锰不溶于水,钨酸钠易溶于水判断A为钨酸钠;钨酸钠和浓盐酸反应生成钨酸和氯化钠;钨酸酸性很弱,难溶于水,判断B为钨酸;钨酸加热分解产生三氧化钨的水,判断C为三氧化钨;
(3)根据碳还原氧化钨生成钨、CO或CO2;钨的熔点很高,不容易转变为液态,碳或氢气都可置换出钨,但碳为固体,难以分离;
(4)根据蓝色氧化钨中钨的质量分数为0.7985来计算求出x;把五价和六价两种价态的氧化物的化学式分别写成WO2.5和WO3,设蓝色氧化钨的组成为xWO2.5?yWO3,利用W和O的个数之比为1:2.90来解答;
(2)根据氢氧化铁和氢氧化锰不溶于水,钨酸钠易溶于水判断A为钨酸钠;钨酸钠和浓盐酸反应生成钨酸和氯化钠;钨酸酸性很弱,难溶于水,判断B为钨酸;钨酸加热分解产生三氧化钨的水,判断C为三氧化钨;
(3)根据碳还原氧化钨生成钨、CO或CO2;钨的熔点很高,不容易转变为液态,碳或氢气都可置换出钨,但碳为固体,难以分离;
(4)根据蓝色氧化钨中钨的质量分数为0.7985来计算求出x;把五价和六价两种价态的氧化物的化学式分别写成WO2.5和WO3,设蓝色氧化钨的组成为xWO2.5?yWO3,利用W和O的个数之比为1:2.90来解答;
解答:解:(1)74W的质子数可知电子数为74,核外各电子层电子数为2、8、18、32、14、2,电子层数等于周期序数,所以在周期表的位置是第六周期;
故答案为:六;
(2)氢氧化铁和氢氧化锰不溶于水,钨酸钠易溶于水判断A为钨酸钠;钨酸钠和浓盐酸反应生成钨酸(H2WO4)和氯化钠;钨酸(H2WO4)酸性很弱,难溶于水,判断B为钨酸(H2WO4);钨酸(H2WO4)加热分解产生三氧化钨(WO3)的水,判断C为三氧化钨(WO3);
故答案为:H2WO4;WO3;
(3)碳还原氧化钨生成钨、CO或CO2,反应的方程式为WO3+3C=W+3CO或2WO3+3C═2W+3CO2,
故答案为:WO3+3C
W+3CO↑或2WO3+3C
2W+3CO2↑;
碳或氢气都可置换出钨,钨的熔点很高,不容易转变为液态,如果用碳作还原剂,混杂在金属中的碳不易除去,而且碳在高温下和金属钨也能生成碳化钨,不容易获得纯净的金属钨,H2作还原剂,过量的H2会从体系中自动逸出;
故答案为:因为钨的熔点很高,不容易转变为液态,如果用碳做还原剂,混杂在金属中的碳不易除去,而且碳会在高温下和金属钨反应形成碳化钨,不容易获得纯的金属钨,用氢气作还原剂就不存在这些问题;
(4)①WO3-x中钨的质量分数为
=0.7985,解得x=0.10;
故答案为:0.10;
②把五价和六价两种价态的氧化物的化学式分别写成WO2.5和WO3,设蓝色氧化钨的组成为xWO2.5?yWO3,
因W和O的个数之比为1:2.90,则有
=
,解得
=
,所以蓝色氧化钨中五价和六价两种价态的钨的原子数之比为:1:4;
故答案为:六;
(2)氢氧化铁和氢氧化锰不溶于水,钨酸钠易溶于水判断A为钨酸钠;钨酸钠和浓盐酸反应生成钨酸(H2WO4)和氯化钠;钨酸(H2WO4)酸性很弱,难溶于水,判断B为钨酸(H2WO4);钨酸(H2WO4)加热分解产生三氧化钨(WO3)的水,判断C为三氧化钨(WO3);
故答案为:H2WO4;WO3;
(3)碳还原氧化钨生成钨、CO或CO2,反应的方程式为WO3+3C=W+3CO或2WO3+3C═2W+3CO2,
故答案为:WO3+3C
| ||
| ||
碳或氢气都可置换出钨,钨的熔点很高,不容易转变为液态,如果用碳作还原剂,混杂在金属中的碳不易除去,而且碳在高温下和金属钨也能生成碳化钨,不容易获得纯净的金属钨,H2作还原剂,过量的H2会从体系中自动逸出;
故答案为:因为钨的熔点很高,不容易转变为液态,如果用碳做还原剂,混杂在金属中的碳不易除去,而且碳会在高温下和金属钨反应形成碳化钨,不容易获得纯的金属钨,用氢气作还原剂就不存在这些问题;
(4)①WO3-x中钨的质量分数为
| 183.84 |
| 183.84+16×(3-x) |
故答案为:0.10;
②把五价和六价两种价态的氧化物的化学式分别写成WO2.5和WO3,设蓝色氧化钨的组成为xWO2.5?yWO3,
因W和O的个数之比为1:2.90,则有
| x+ y |
| 2.5x+ 3y |
| 1 |
| 2.90 |
| x |
| y |
| 1 |
| 4 |
点评:本题主要考查工业制备流程、金属的冶炼和化学计算,题目难度不大,本题注意判断A、B、C三种物质.

练习册系列答案
相关题目