题目内容
黑火药是中国古代四大发明之一,它的爆炸反应为:
2KNO3+3C+S A+N2↑+3CO2↑(已配平)。
A+N2↑+3CO2↑(已配平)。
(1)生成物中除了氮气与二氧化碳外,还有一种物质A,则A的电子式为 ,A属于________化合物。
(2)黑火药中位于元素周期表短周期的元素有 种。其中一种元素的单质可用于制药,其氧化物可用于漂白织物和作防腐剂,该元素在周期表中的位置是 。
(3)黑火药中所含元素的原子半径从大到小的顺序是 (用元素符号表示);
(4)下列事实能说明黑火药中碳与硫两元素非金属性相对强弱的有 。
A.同条件同浓度溶液的pH:Na2CO3>Na2SO4
B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
(1)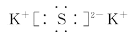 离子
离子
(2)4 第三周期第ⅥA族
(3)K>S>C>N>O (4)A、C
【解析】(1)根据原子守恒可知A为K2S,其电子式为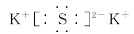 ,属于离子化合物。
,属于离子化合物。
(2)黑火药中位于元素周期表短周期的元素有C、N、O 、S四种。其中硫元素位于周期表中第三周期第ⅥA族,其单质可用于制药,SO2可用于漂白织物和作防腐剂。
(3)黑火药中所含元素的原子半径从大到小的顺序是K>S>C>N>O;
(4)同条件同浓度溶液的pH:Na2CO3>Na2SO4,说明酸性 H2SO4>H2CO3,CS2中碳元素为+4价,硫元素为-2价,说明硫元素原子的得电子能力强,这两个事实都可以说明硫的非金属性比碳强。B项中,H2SO3不是硫元素最高价氧化物对应的水化物。

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目