��Ŀ����
����Ŀ������һ����Ҫ�Ľ�������������[��Ҫ�ɷ�Ϊ����������FeTiO3��������������Fe2O3]Ϊԭ���Ʊ��ѵĹ���������ͼ��ʾ��

��1����Һ1����Ԫ����TiO2+��ʽ���ڣ����ܽ������̷�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ________��
��2������AΪ________���ѧʽ������һϵ�в�����Ϊ________��
��3����ˮ�⡱����������TiO2��xH2O��Ϊ���TiO2��xH2O�IJ��ʣ��ɲ�ȡ�Ĵ�ʩ��________��________����д����������
��4������⡱����ʯīΪ������TiO2Ϊ����������CaOΪ����ʡ������ĵ缫��ӦʽΪ________�����Ƶý���Ti 9.60g��������������________mL����״���£���
��5��������FeSO4��7H2O����ˮ������һ������NaHCO3��Һ�����Ƶ�FeCO3��д����Ӧ�����ӷ���ʽ________������Ӧ�����Һ��c��Fe2+��=2��10-6mol��L-1������Һ��c��CO32-��=________mol��L-1������֪��������FeCO3������ҺŨ��Ϊ4.5��10-6mol��L-1��
���𰸡�FeTiO3��2H2SO4 ![]() TiOSO4��FeSO4��2H2O Fe ����Ũ������ȴ�ᾧ������ ��ˮϡ�ͷ�Ӧ�� �Ӽ��к����ɵ��ᡢ���ȵ� TiO2��4e��===Ti��2O2�� 4480��2�֣� Fe2+ + 2HCO3����FeCO3��+CO2��+ H2O 1��10��5
TiOSO4��FeSO4��2H2O Fe ����Ũ������ȴ�ᾧ������ ��ˮϡ�ͷ�Ӧ�� �Ӽ��к����ɵ��ᡢ���ȵ� TiO2��4e��===Ti��2O2�� 4480��2�֣� Fe2+ + 2HCO3����FeCO3��+CO2��+ H2O 1��10��5
��������
����������ᷴӦ���������Ѻ����������������������ᷴӦ������������ˮ��������������̷��������м��������ӱ���������ӵĹ��̣����Լ�������AΪ��������������Һͨ������Ũ������ȴ�ᾧ�����˵õ������������塣���ݵ���������ʧȥ���ӷ���������Ӧ�������õ����ӷ�����ԭ��Ӧ�����缫��Ӧ����ʽ��
��1������������Ҫ�ɷ�ΪFeTiO3������Һ1����Ԫ����TiO2+��ʽ���ڣ���������Ҫ��Ӧ��ѧ����ʽΪFeTiO3��2H2SO4 ![]() TiOSO4��FeSO4��2H2O��
TiOSO4��FeSO4��2H2O��
��2���������л��и�����FeSO4��7H2O�����轫�ܽ������е�Fe3+��ȥ������AΪFe����һϵ�в�������������Ũ������ȴ�ᾧ�����ˡ�
��3�� ��ˮ�⡱��ӦΪTiO2����(x��1)H2O===TiO2��xH2O����2H��������ƽ���ƶ�ԭ����Ϊ���TiO2��xH2O�IJ��ʿ��Լ�ˮϡ�ͷ�Ӧ��Ӽ��к����ɵ��ᡢ���ȵȡ�
��4������⡱������������Ӧ��TiO2��4e��===Ti��2O2����������Ӧ��2O2����4e��===O2�������Ƶý���Ti 9.60g����n(Ti)=n(O2)=0.2mol��V(O2)=4480mL����״���£���
��5��������֪�÷�Ӧ��ѧ����ʽΪ��Fe2+ + 2HCO3����FeCO3��+CO2��+ H2O���ɳ�����FeCO3������ҺŨ��Ϊ4.5��10��6 mol��L-1��KSP(FeCO3)=2.025��10��11 mol2��L-2����c(CO32��)��![]() = 1.013��10��5mol��L-1��
= 1.013��10��5mol��L-1��

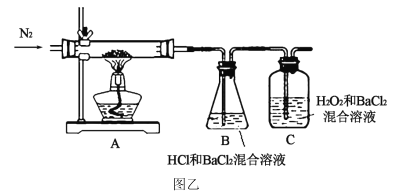
����Ŀ����.������KMnO4��H2C2O4(����)��Ӧ�о�Ӱ�췴Ӧ���ʵ����أ����ӷ���ʽΪ2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O��һʵ��С����ͨ���ⶨ��λʱ��������CO2�����ʣ�̽��ij��Ӱ�컯ѧ��Ӧ���ʵ����أ����ʵ�鷽������(KMnO4��Һ���ữ)��
ʵ����� | A��Һ | B��Һ |
�� | 20mL 0.1mol��L-1H2C2O4��Һ | 30mL 0.1 mol��L-1KMnO4��Һ |
�� | 20mL 0.2mol��L-1H2C2O4��Һ | 30mL 0.1mol��L-1KMnO4��Һ |
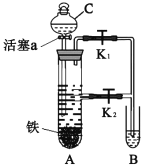
��1����ʵ��̽������____���ضԻ�ѧ��Ӧ���ʵ�Ӱ�졣��ͼһ����ͬʱ������Ͳ�����õ�CO2�����С��ϵ��___����ʵ����ţ���

��2����ʵ�����2minĩ�ռ���2.24mLCO2(��״����)������2minĩ��c(MnO4-)___ mol��L-1(������Һ���Ϊ50mL)��
��3����ͨ���ⶨһ��ʱ����CO2��������ȽϷ�Ӧ�����⣬��ʵ�黹��ͨ���ⶨ___���Ƚϻ�ѧ��Ӧ���ʡ�
��4��С��ͬѧ���ַ�Ӧ����������ͼ��������t1��t2ʱ�������ʱ�����Ҫԭ������Ǣٲ���MnSO4�Ǹ÷�Ӧ�Ĵ�������_____��
��.һ���¶��£���һ������N2��H2����̶�������ܱ������н��з�Ӧ��
N2(g)+3H2(g)![]() 2NH3(g)��
2NH3(g)��
��1������������˵���ÿ��淴Ӧ�ﵽ��ѧƽ��״̬����___��
A.�����ڵ�ѹǿ����
B.������������ܶȲ���
C.��ͬʱ������3mol H-H�����ѣ���6mol N-H���γ�
D.c(N2)��c(H2)��c(NH3)��1��3��2
E.NH3�������������ٸı�
��2������ʼʱ�������г���10mol ��L-1��N2��15mol ��L-1��H2��10minʱ���������NH3��Ũ��Ϊ1.5mol ��L-1��10min����N2��ʾ�ķ�Ӧ����Ϊ___����ʱH2��ת����Ϊ___��