题目内容
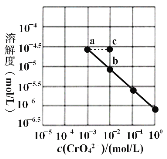
【题目】已知溶解度也可用物质的量浓度表示,25℃时,Ag2CrO4在不同浓度CrO42-溶液中的溶解度如图所示。又知Ksp(AgCl)=1.8×10-10。下列说法正确的是
A.图中a、b两点c(Ag+)相同
B.该温度下,Ag2CrO4溶度积的数量级为10-12
C.加热蒸发饱和Ag2CrO4溶液再恢复到25℃,可使溶液由a点变到b点
D.将0.01 mol/L AgNO3溶液滴入20mL0.01 mol/L KCl和0.01 mol/L K2CrO4的混合溶液中,CrO42-先沉淀
【答案】B
【解析】
A.曲线为达到沉淀溶解平衡时的曲线,a点和b点c(CrO42-)不一样,则c(Ag+)不相同,A错误;
B. 根据图象上相关数据,Ag2CrO4(s)![]() 2Ag+(aq)+CrO42-(aq),如以c(CrO42-)=10-2 mol/L时,溶解度为10-5 mol/L计算Ksp=c2(Ag+) c(CrO42-)=(2×10-5)2×10-2=4×10-12,则数量级为10-12,B正确;
2Ag+(aq)+CrO42-(aq),如以c(CrO42-)=10-2 mol/L时,溶解度为10-5 mol/L计算Ksp=c2(Ag+) c(CrO42-)=(2×10-5)2×10-2=4×10-12,则数量级为10-12,B正确;
C. 加热蒸发饱和Ag2CrO4溶液再恢复到25℃,仍然为该温度下的饱和溶液,各种微粒的浓度不变,因此不能使溶液由a点变到b点,C错误;
D. 由于Ksp(AgCl)=1.8×10-10,当溶液中KCl为0.01 mol/L时,形成沉淀需Ag+的浓度最小为c(Ag+)=![]() mol/L=1.8×10-8 mol/L,而Ksp(Ag2CrO4)=4×10-12,形成Ag2CrO4时需要Ag+的浓度最小为c(Ag+)=
mol/L=1.8×10-8 mol/L,而Ksp(Ag2CrO4)=4×10-12,形成Ag2CrO4时需要Ag+的浓度最小为c(Ag+)=![]() mol/L=2×10-5 mol/L,形成沉淀需要的Ag+浓度越小,先形成沉淀,可见等浓度的混合溶液中,Cl-先产生沉淀,D错误;
mol/L=2×10-5 mol/L,形成沉淀需要的Ag+浓度越小,先形成沉淀,可见等浓度的混合溶液中,Cl-先产生沉淀,D错误;
故合理选项是B。

【题目】以低品位红土镍矿(主要成分可表示为![]() 、
、![]() 、
、![]() ,含有少量
,含有少量![]() 、
、![]() 、
、![]() 、
、![]() )为原料制备纳米级
)为原料制备纳米级![]() 的工艺流程如下:
的工艺流程如下:

已知氢氧化物的参数如下表:
氢氧化物 | 溶度积 | 开始沉淀 | 完全沉淀 |
|
| 4.1 | 5.5 |
|
| 2.2 | 3.5 |
|
| 6.7 | 9.5 |
|
| 9.4 | 12.4 |
回答下列问题:
(1)“滤渣Ⅰ”的主要成分是______(填化学式)。
(2)常温下,调![]() 的目的是______。当
的目的是______。当![]() 时,溶液中
时,溶液中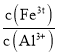 =______
=______
(3)写出“除铜镍”过程发生反应的离子方程式为![]() 、______________。“除钙”过程反应温度不宜超过
、______________。“除钙”过程反应温度不宜超过![]() 的原因_________________________。
的原因_________________________。
(4)“滤液”中溶质的主要成分为________________,获取该物质晶体的具体实验操作为__________。
【题目】在恒容条件下化学反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-QkJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如表所列:
2SO3(g) ΔH=-QkJ·mol-1,在上述条件下分别充入的气体和反应放出的热量(Q)如表所列:
容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根据以上数据,下列叙述正确的是( )
A.在上述条件下反应生成1molSO3固体放热![]() kJ
kJ
B.2Q1<2Q2=Q1<Q
C.Q1=2Q2=2Q3=Q
D.2Q2=2Q3<Q1<Q